سندرم نفروتیک وضعیتی است که با آسیب به سلول های پادوسیت مشخص می شود که منجر به پروتئینوری قابل توجه، ادم، چربی خون و افزایش انعقاد می شود. عفونت ها و بدخیمی ها اغلب با سندرم نفروتیک همراه هستند. ویروس COVID-19 با چندین تظاهرات غیر معمول شامل عفونت های تنفسی فوقانی و آسیب حاد کلیه همراه است. با توجه به اینکه COVID-19 باعث تغییرات التهابی سیستمیک می شود، به نظر می رسد که ممکن است منجر به سندرم نفروتیک شود. این مطالعه با هدف بررسی وجود ارتباط بین COVID-19 و انواع مختلف سندرمهای نفروتیک انجام شد. تجزیه و تحلیل آماری با استفاده Statistical Package for Social Sciences (SPSS، IBM Corp.، Armonk، نیویورک، ایالات متحده آمریکا) انجام شد.
ما یک جستجوی سیستماتیک در پایگاههای اطلاعاتی PubMed/Medline و Embase با استفاده از سرفصلهای موضوعی پزشکی (MeSH) و کلمات کلیدی معمولی مرتبط با COVID-19 و سندرم نفروتیک، از جمله انواع مختلف سندرمهای نفروتیک، انجام دادیم. جستجو در ۱۷ دسامبر ۲۰۲۱ انجام شد. ما کیس ریپورت ها و مجموعهای از بیماران بزرگسال که در مدت کوتاهی پس از عفونت یا واکسیناسیون یافتههای نشاندهنده سندرم نفروتیک داشتند، اضافه کردیم. ما موارد مربوط به کودکان، زنان باردار، مقالاتی که به زبانهایی غیر از انگلیسی نوشته شده بودند و مواردی که قابل بازیابی نبودند را حذف کردیم. ارتباط و کیفیت مقالات شناسایی شده مورد ارزیابی قرار گرفت.
ما ۳۲ مقاله را در این مطالعه گنجاندیم که عمدتاً شامل کیس ریپورت های موردی و سریال بوده است. در مطالعه ما، کووید-۱۹ و واکسن کووید-۱۹ با ایجاد سندرم نفروتیک (عمدتاً فرم در حال کلاپس گلومرولواسکلروز سگمنتال کانونی ) مرتبط بوده است، اگرچه اشکال دیگری نیز مشاهده شده است. در تاریخچه بیمار، تظاهرات بالینی، دورههای بالینی یا رژیمهای درمانی سازگار کمی وجود داشت، اگرچه به نظر میرسید که اکثر این اختلالات در نهایت برطرف شدند اما قبل از اینکه بتوان به نتایج قطعی تری رسید، موارد بیشتری باید گزارش و تجزیه و تحلیل شود.
در نتیجه، سندرم نفروتیک یک عارضه احتمالی عفونت COVID-19 و واکسن COVD-19 است و باید در بیمارانی که ادم های شروع ناگهانی یا بدتر شدن عملکرد کلیه را نشان می دهند در نظر گرفته شود. در حالی که اکثر موارد به درمان استاندارد پاسخ میدهند اما زمانی که دادههای بیشتری در دسترس قرار گرفت، باید دستورالعملهای واضحتری ایجاد شود.
مقدمه و پیشینه
شیوع پنومونی با علت ناشناخته در دسامبر ۲۰۱۹ در ووهان چین کشف شد. نمونههایی از بیماران مبتلا بهدست آمد و تجزیه و تحلیل مولکولی یک ویروس کرونای جدید را نشان داد که در ابتدا ۲۰۱۹-nCoV نام داشت و متعاقباً توسط سازمان بهداشت جهانی (WHO) به COVID-19 تغییر نام داد. این سویه جدید کروناویروس هفتمین عضو از خانواده coronaviridae است که می تواند انسان را آلوده کند. این یک ویروس بسیار بیماری زا و مسری است که سازمان بهداشت جهانی را بر آن داشت تا در ۳۰ ژانویه ۲۰۲۰ آن را به عنوان یک وضعیت اضطراری عمومی و نگرانی بین المللی و تا ۱۱ مارس ۲۰۲۰ یک بیماری همه گیر اعلام کند. علاوه بر این، تا ۸ آگوست ۲۰۲۲، ۵۹۱,۴۰۷,۹۷۸ مورد تایید شده کووید-۱۹ در سراسر جهان ثبت شده است که ۶,۴۴۲,۲۰۴ مورد مرگ گزارش شده است. اگرچه چندین مسیر انتقال شناخته شده است اما قطرات تنفسی و تماس نزدیک راههای اصلی انتقال هستند. شایع ترین علائم تظاهر کننده تب، از دست دادن بویایی، سرفه و خستگی است و درصد کمی از بیماران با آسیب شدید اندام و/یا مرگ مراجعه می کنند.
از آغاز همهگیری، اقدامات متعددی برای کاهش شیوع ویروس اجرا شده است، از جمله فاصلهگذاری اجتماعی، استفاده از ماسک و قرنطینههای منطقهای. علاوه بر این، چندین درمان مورد مطالعه قرار گرفت، مانند داروهای ضد ویروسی (یعنی لوپیناویر، ریتوناویر و رمدسیویر) که تا حدی اثربخشی در برابر ویروس نشان دادند، و تعدیلکنندههای ایمنی (به عنوان مثال، توسیلیزوماب، اکولیزوماب، دگزامتازون، کلشی سین) که به نظر میرسد حالت پرالتهابی را که ثانویه به طوفان سیتوکین ناشی از این بیماری ویروسی است را کاهش میدهند. با این حال، از آنجایی که هیچ دارویی وجود ندارد که مستقیماً ویروس را از بین ببرد، واکسن ها آخرین امید برای متوقف کردن این بیماری همه گیر شدند. در نتیجه، سازمان غذا و دارو (FDA) مجوز استفاده اضطراری برای واکسن Pfizer-BioNTech (Cominarty/BNT162b2) را در ۱۱ دسامبر ۲۰۲۰ صادر کرد. برای واکسن مدرنا (mRNA-1273) در ۱۸ دسامبر ۲۰۲۰؛ و برای واکسن جانسون جانسون (JNJ-78436735) در ۲۷ فوریه ۲۰۲۱.
Pfizer-BioNTech و Moderna که به ترتیب دارای اثربخشی ۹۵% و ۹۴.۱% هستند، واکسنهای پیامرسان ریبونوکلئیک اسید (mRNA) هستند که باعث ایجاد پاسخ ایمنی در برابر پروتئین اسپایک COVID-19 میشوند. واکسن ها mRNA حاوی نانوذرات لیپیدی هستند که از طریق اندوسیتوز وارد سلول می شوند. هنگامی که mRNA در سیتوپلاسم قرار می گیرد، از آندوزوم و نانوذره لیپیدی که mRNA را از تخریب محافظت می کند، می گریزد و توسط ریبوزوم ها به پروتئین اسپایک تبدیل می شود. بعداً، پروتئین اسپایک یکی از دو مسیر را دنبال میکند: ۱) تا حدی در پروتئازومها به پپتیدها تجزیه میشود، سپس برای تعامل با سلولهای ایمنی روی کمپلکس اصلی سازگاری بافتی (MHC) کلاس I بارگذاری میشود. یا ۲) در فضای خارج سلولی ترشح می شود، از طریق اندوسیتوز به سلول های ارائه دهنده آنتی ژن وارد می شود، در MHC کلاس II نمایش داده می شود و به سلول های ایمنی ارائه می شود که شروع به تولید آنتی بادی علیه COVID-19 می کنند. واکسن جانسون جانسون یک واکسن ناقل ویروسی با اثربخشی ۶۶.۳ درصد است که از یک ویروس مهندسی شده با تکثیر برای بیان توالی ژنتیکی آنتی ژن مورد نظر در سلول های میزبان استفاده می کند.
شایع ترین عوارض جانبی واکسن کووید-۱۹ شامل درد، تورم و قرمزی در بازوی محل تزریق واکسن و همچنین خستگی، درد عضلانی، سردرد، تب، لرز و حالت تهوع است. علاوه بر این، عوارض جانبی شدید کمتری مانند سندرم نفروتیک که شرایطی بالینی است با با پروتئینوری، هیپوآلبومینمی، ادم و چربی خون و سایر عوارض نیز به چشم میخورد. این مرور سیستماتیک چندین مورد از سندرم نفروتیک را نشان میدهد که پس از عفونت با کووید یا واکسیناسیون ایجاد میشود. اگرچه مکانیسم دقیق سندرم نفروتیک در این شرایط هنوز مشخص نشده است اما شکل گیری فرضیه های مرتبط در حال افزایش است. ارزیابی میکروسکوپی نمونههای کلیه در برخی از بیماران ذرات کروی شبیه ویروس را در سیتوپلاسم پودوسیتها نشان داده است که نشاندهنده یک اثر سیتوپاتیک مستقیم ویروسی، مشابه گلومرولوپاتی مرتبط با HIV است. فرضیه دیگر این است که گیرندههای آنزیم ۲ مبدل آنژیوتانسین (که به تهاجم کووید-۱۹ به سلولهای هدف کمک میکنند) موجود در پودوسیتها و لولههای پیچخورده پروگزیمال میتوانند تمایل این سلولها را به تأثیرپذیری توضیح دهند. بنابراین، پزشکان باید ارتباط احتمالی بین سندرم نفروتیک و عفونت / واکسیناسیون کووید-۱۹ را در نظر بگیرند تا بتوانند نسبت به وجود علائم هوشیار باشند و برای مدیریت مناسب آماده باشند.
مرور
مواد و روش ها
این مقاله از دستورالعملهای گزارشدهی ترجیحی برای بررسیهای سیستماتیک و متاآنالیز (PRISMA) برای بررسیهای سیستماتیک پیروی میکند. یک جستجوی متون سیستماتیک با استفاده از پایگاههای اطلاعاتی PubMed/Medline و Embase انجام شد. جستجو از ابتدا تا ۱۷ دسامبر ۲۰۲۱ انجام شد. از استراتژی جستجوی زیر و ترکیبی از عبارات و کلمات کلیدی معمولی عناوین موضوع پزشکی (MeSH) استفاده شد: (“COVID-19″[Mesh] یا “SARS-CoV-2″[Mesh ] یا «واکسنهای COVID-19» [مش] یا «واکسن BNT162» [مش] یا «واکسن ۲۰۱۹-nCoV mRNA-1273» [مش] یا «Ad26COVS1»[Mesh] یا «COVID19» یا «COVID» یا «COVID» ۲۰۱۹ یا «کرونا ویروس جدید» یا «SARS-CoV-2» یا «کروناویروس جدید» یا «COVID2019» یا «واکسنهای COVID2019» یا «واکسنهای mRNA» یا «واکسنهای کروناویروس» یا «واکسنهای SARS-CoV-2» یا «Pfizer» واکسن” یا “واکسن Pfizer-BioNTech” یا “واکسن مدرنا” یا “واکسن یانسن” یا “واکسن جانسون و جانسون”) و (“سندرم نفروتیک” [مش] یا “گلومرولواسکلروز، بخش کانونی” [مش] یا “نفروسیس” لیپویید» [مش] یا «گلومرولونفریت، غشایی» [مش] یا «سندرم نفروتیک» یا «گلومرولوسکلروزیس سگمنتال کانونی» یا «گلومرولونفریت اسکلروزان کانونی» یا «FSGS» یا «بیماری با تغییرات حداقلی» یا «نفیل بافتی غشایی» “).
نتایج به پلتفرم Covidence منتقل شد که موارد تکراری را به طور خودکار حذف کرد. دو داور مستقل مقالات را در دو مرحله ارزیابی کردند، ابتدا تنها با بررسی عناوین و چکیدهها و سپس تجزیه و تحلیل متن کامل. تضادها از طریق ارتباط مستقیم بین داوران یا با رای داور سوم حل شد. ما تمام موارد سندرم نفروتیک از قبل موجود و موارد مربوط به کودکان یا زنان باردار را حذف کردیم. ما همچنین مقالاتی را که به زبانهای دیگری غیر از انگلیسی نوشته شده بودند حذف کردیم. مطالعه ما گزارشهای موردی، سریهای موردی، مطالعات مقطعی، مورد شاهدی آیندهنگر و گذشتهنگر و مطالعات کوهورت را شامل شد. مرورها و متاآنالیزها حذف شدند. ارزیابی کیفیت با استفاده از مقیاس نیوکاسل-اتاوا برای مطالعات مورد-شاهدی و کوهورت و “چک لیست گزارشهای موردی – موسسه جوآنا بریگز” برای گزارشهای موردی و کیس ریپورت های سریال انجام شد. ما مطالعاتی را وارد کردیم که در هر مقیاس حداقل دو امتیاز کمتر از حداکثر داشتند. چکیده ها در صورتی گنجانده می شدند که شرایط کیفی مشابه نسخه های اصلی را داشته باشند. برای استخراج دادهها از یک بستر گسترده استفاده شد و ویژگیهای مرتبط ارائههای بیماران، مقادیر آزمایشگاهی و دورههای بیماری همانطور که در مطالعه اصلی گزارش شده بود، ثبت شد. در صورت امکان، مقادیر آزمایشگاهی به واحدهای ایالات متحده تبدیل شد. سپس داده ها مورد تجزیه و تحلیل قرار گرفت و به صورت توصیفی گزارش شد. میانگین و انحراف معیار برای متغیرهای عددی با استفاده از نرم افزار SPSS محاسبه شد. یافته ها در جداول ایجاد شده ارائه شد. هیچ فرضی انجام نشد و هر داده ای که مستقیماً گزارش نشده بود به عنوان غیرقابل اجرا ثبت شد (NA). هر تجزیه و تحلیل فقط در میان مطالعاتی انجام شد که در آن متغیر مورد نظر گزارش شده بود.
نتایج
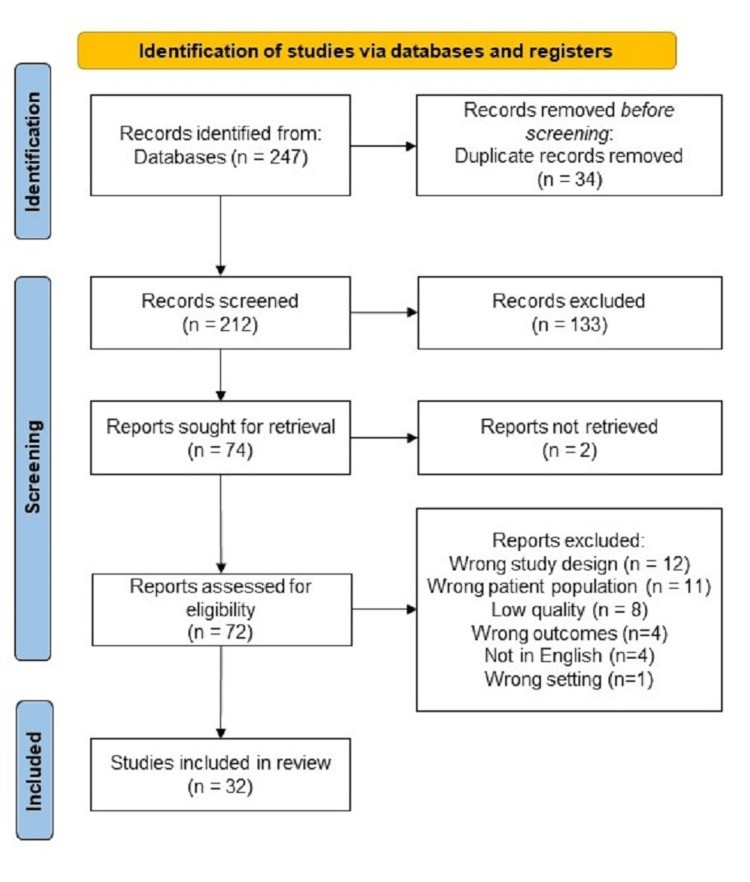
در مجموع ۲۴۷ مطالعه از پایگاه داده های Medline/PubMed و Embase وارد شد و ۳۴ مورد تکراری حذف شد و ۲۱۲ مطالعه برای غربالگری باقی ماند. دو بازبین مستقل ۱۳۳ مورد از این مطالعات را نامربوط تشخیص دادند، و ۷۴ مورد برای متن کامل غربالگری شدند. از این تعداد، ۳۲ مورد در تحلیل نهایی قرار گرفتند (شکل ۱) . ما ۱۲ مطالعه را حذف کردیم زیرا طرحهای مطالعه نادرست بودند، ۱۱ مطالعه را به دلیل اینکه مربوط به جامعه آماری نادرستی بود و هشت مورد را به دلیل اینکه الزامات ارزیابی کیفیت را برآورده نمیکردند حذف کردیم. دلایل بیشتر حذف نیز شامل نتایج متفاوتی نسبت به آنچه در حال مطالعه ماست بود مثل زبانهایی غیر از انگلیسی، جمعیت اطفال و نداشتن اطلاعات بعدی بود. هیچ سوگیری آشکاری شناسایی نشد. ما داده ها را در یک صفحه گسترده استخراج کردیم و اطلاعات دموگرافیک (سن، جنسیت، قومیت)، سابقه پزشکی مرتبط (سابقه بیماری مزمن کلیوی (CKD)، بدخیمی ها، عفونت های مزمن، استفاده از داروهای ضد التهابی غیر استروئیدی، پیوند کلیه) ،داده های آزمایشگاهی مربوطه در مورد تظاهر و در ابتدا (کراتینین سرم، آلبومین سرم، پروتئین ادرار)، دوره بیماری، از جمله تعداد جلسات همودیالیز، تعداد پذیرش در بخش مراقبت های ویژه (ICU) و تعداد درمان های مربوطه تجویز شده را جمع آوری کردیم. داده های پیگیری شامل بررسی وجود نیاز به همودیالیز و بررسی کراتینین سرم و پروتئین ادرار در هنگام ترخیص بود. همه واحدها به واحدهایی که معمولاً در ایالات متحده استفاده می شوند تبدیل شدند. برای برخی از متغیرها، تبدیل غیرممکن بود و همانطور که در مطالعه اصلی گزارش شده بود، ثبت شدند.
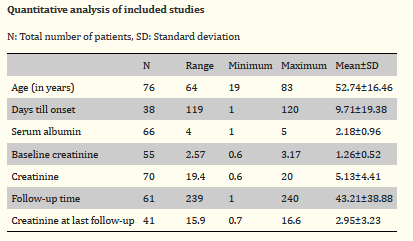
در مجموع ۷۶ بیمار در این مطالعه وارد شدند که ۵۶ نفر (۳/۷۳%) مرد و ۲۰ نفر (۳/۲۶%) زن بودند. میانگین سنی نمونه ۱۶.۴±۵۲.۷ سال و بین ۱۹ تا ۸۳ سال است (جدول ۱).
شایع ترین نژادها در بین بیماران به شرح زیر است: ۳۵ (۴۶.۱%) بیمار آفریقایی آمریکایی و ۱۹ (۲۵%) بیمار قفقازی. در مجموع ۵۰ نفر (۶۵.۸٪) عفونت COVID-19 را تأیید کرده بودند و ۴۶ (۹۲٪) علامتدار بودند. ۲۶ بیمار (۳۴.۲%) واکسن کووید-۱۹ را دریافت کرده بودند. علائم بعد از اولین دوز واکسن در ۱۵ نفر (۷/۱۹%) و بعد از دوز دوم در ۱۰ نفر (۲/۱۳%) شروع شد.
پنج بیمار (۶.۶%) سابقه پیوند کلیه داشتند. عفونت مزمن در شش مورد (۷.۹%) (ویروس هپاتیت C (HCV)، ویروس نقص ایمنی انسانی (HIV)، ویروس هپاتیت B (HBV)، مالاریا، شیستوزومیازیس و عفونت استرپتوکوک گزارش شد. ۵۶ بیمار (۷۳.۳%) فاقد CKD، ۱۲ (۱۵.۷%) CKD گزارش شده بودند و ۸ مورد دچار (۱۰.۵%) به بیماری کلیوی مرحله نهایی (ESRD) گزارش شده بودند. سه بیمار سرطان پروستات داشتند. دو مورد سرطان دهانه رحم و یک مورد مایکوزیس قارچی پوستی وجود داشت. استفاده از داروهای ضد التهابی غیر استروئیدی (NSAID) تنها در یک مورد گزارش شده است.
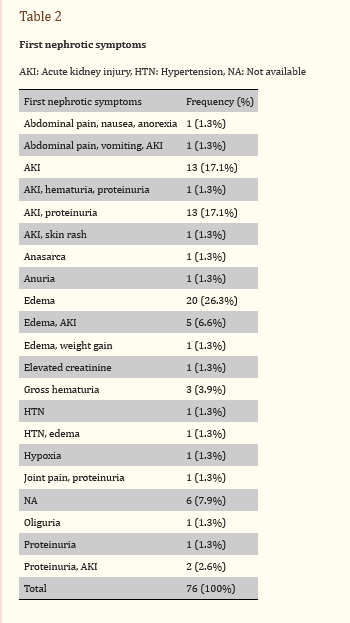
از بین ۷۶ مورد گزارش شده، تنها در ۳۸ مورد، فاصله بین عفونت یا واکسیناسیون و شروع سندرم نفروتیک گزارش شده است. میانگین فاصله ۹.۷۱±۱۹.۳۷ روز است. این از یک روز تا چهار ماه متغیر است. فقط یک بیمار نیاز به بستری در مراقبت های ویژه داشت. در زمان ارائه، ۳۶ بیمار آسیب حاد کلیه (AKI) داشتند. بیست و هفت (۳۵.۵%) از بیماران با ادم مراجعه کردند. هر دو AKI و پروتئینوری در ۱۵ بیمار (۱۹.۷٪) مشاهده شد. سه بیمار با هماچوری شدید مراجعه کردند. دو بیمار با آنوری/الیگوری و یک بیمار با آناسارکا (جدول ۲).
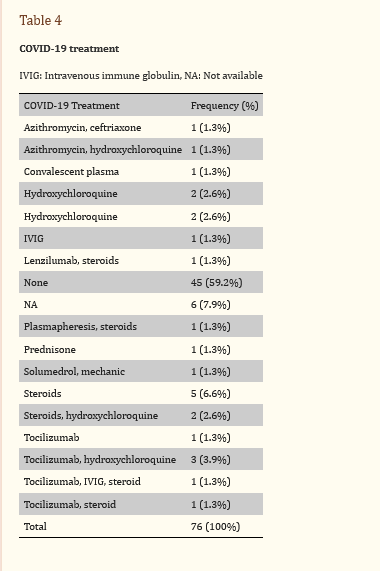
میانگین سطح آلبومین سرم در گروه بیماران ۹۶/۰±۱۸/۲ گرم در دسی لیتر بود. میانگین غلظت پایه کراتینین برای بیماران شرکتکننده در این مطالعه ۰.۵۱±۱.۲۵ میلیگرم در دسیلیتر است. میانگین سطح کراتینین سرم ۴.۴۱±۵.۱۳ میلی گرم در دسی لیتر است. بیوپسی کلیه نشان داد که دو بیمار دارای غشای پایه ضد گلومرولی (GBM) و ۲۴ بیمار دارای گلومرولواسکلروز سگمنتال کانونی در حال فروپاشی (FSGS) بودند. سیزده بیمار بیماری حداقل تغییر (MCD) داشتند. ۹ بیمار نفروپاتی غشایی داشتند. پنج بیمار نفروپاتی ایمونوگلوبولین A (IgA) داشتند (جدول (جدول ۳). درمان کووید-۱۹ شامل توسیلیزوماب برای شش بیمار، هیدروکسی کلروکین برای هفت بیمار، پلاسما برای یک بیمار و استروئید برای ۹ بیمار بود.
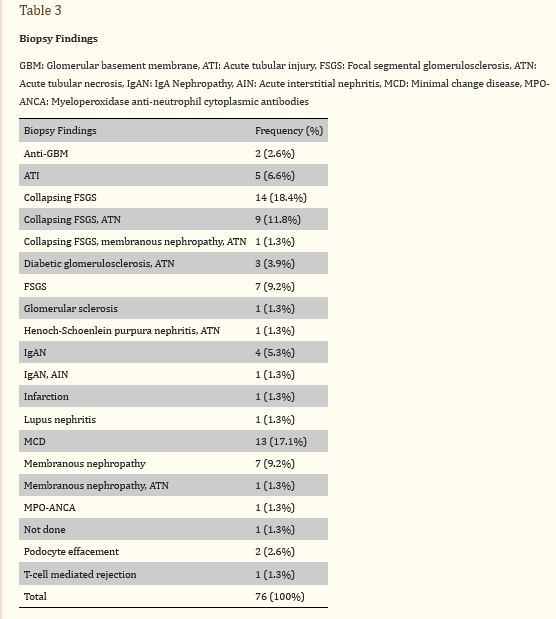
برای درمان سندرم نفروتیک، به ۹ بیمار مهارکننده های آنزیم مبدل آنژیوتانسین (ACE)، به هشت بیمار دیورتیک و پنج بیمار مورد همودیالیز قرار گرفتند. سی و هشت نفر (۵۱.۳٪) کورتیکواستروئید دریافت کردند، در حالی که ۳۹بیمار (۵۱.۳٪) دریافت نکردند. بیست و چهار بیمار (۱۸.۲۴%) در مدت کوتاهی پس از تشخیص به همودیالیز نیاز داشتند (جدول (جدول ۴). The4). میانگین دوره پیگیری ۸/۳۸±۲۱/۴۳ روز است. با توجه به پیش آگهی، شش بیمار بهبود کامل را تجربه کردند. در ۱۵ بیمار، عملکرد کلیه آنها بدتر شد، هشت نفر ثابت ماندند، ۳۳ بیمار بهبود یافتند و یک نفر فوت کرد. در پیگیری، تنها ۱۶ بیمار (۲۱.۱%) به دیالیز نیاز داشتند. میانگین سطح کراتینین در پیگیری ۲.۹۵±۳.۲۳ میلی گرم در دسی لیتر بود.
بحث
ویژگی های بیمار
در میان مطالعاتی که ما تجزیه و تحلیل کردیم، سندرم نفروتیک هم به دنبال عفونت COVID-19 و هم پس از واکسیناسیون گزارش شده است. با این حال، موارد پس از عفونت بیشتر از پس از واکسن گزارش شده است. از ۷۸ بیمار مورد تجزیه و تحلیل، ۲۶ نفر پس از دریافت واکسن دچار سندرم نفروتیک شدند، در حالی که بقیه به دنبال عفونت با کووید-۱۹ دچار آن شدند. این یافتهها با آنچه که در حال حاضر درباره سایر عوارض ناشی از سیستم ایمنی ناشی از عفونت کووید-۱۹ و واکسنها، مانند میوکاردیت شناخته شده است، مطابقت دارد، که هنوز پس از عفونت بسیار بیشتر از پس از واکسن رخ میدهد .
سن شروع سندرم نفروتیک به طور کلی متفاوت است و انواع مختلف آن در گروه های سنی مختلف شیوع بیشتری دارد. به عنوان مثال، در حالی که MCD در دوران کودکی رایج است، FSGS و نفروپاتی غشایی عموماً در بزرگسالان میانسال و مسنتر رخ میدهد. اکثر بیماران مورد بررسی ما در زمان تشخیص در ۴۰ و ۵۰ سالگی بودند. بیماران بین ۴۰ تا ۶۰ سال تقریباً نیمی از موارد گزارش شده در مطالعات ارائه شده در این بررسی را تشکیل می دهند. با این حال، این نتیجه ممکن است با این واقعیت مخدوش شود که افراد جوانتر به احتمال زیاد از COVID-19 بهبود مییابند بدون اینکه آزمایششان مثبت باشد که البته به دلیل کمبود علائم اختصاصی، و سندرمهای نفروتیک تازه شروع شده آنها ممکن است با COVID-19 مرتبط نباشد. علاوه بر این، FSGS شایع ترین نوع سندرم نفروتیک گزارش شده بود و به طور کلی در بزرگسالان جوان کمتر شایع است. موارد اندکی بیشتر در میان آفریقایی-آمریکایی ها در مقایسه با نژادهای دیگر گزارش شده است، اما این را می توان با تفاوت کلی در بروز FSGS توضیح داد. به طور کلی، تنها ۲۰ مورد در زنان گزارش شده است، در حالی که بقیه در مردان رخ داده است. با این حال، باید توجه داشت که چندین مطالعه بزرگتر، مانند نصر و همکاران. اکثریت قریب به اتفاق موارد خود را در مردان گزارش کردند . علیرغم وجود سندرم نفروتیک در گیرندگان پیوند کلیه، هیچ تفاوتی در پیامدهای مرگ و میر وجود نداشت.
میتوان نتیجه گرفت که ویژگیهای بیمار در میان موارد گزارششده سندرم نفروتیک به دنبال عفونت COVID-19 یا واکسیناسیون با آنچه در هر جمعیتی از بیمارانی که به سندرم نفروتیک مبتلا میشوند، مطابقت دارد. با این حال، باید توجه داشت که مطالعه ما بیماران اطفال را حذف کرد، حتی اگر سندرم نفروتیک، یعنی MCD، در این جمعیت رخ داده باشد. ضمنا کودکان همچنین آخرین جمعیتی بودند که واکسن ضد کووید-۱۹ به آنها تزریق شد. همچنین لازم به ذکر است که دوره ای که واکسن کووید-۱۹ در دسترس بوده است، تنها نیمی از زمان شروع کووید-۱۹ را تشکیل می دهد و تعداد دوزهای کووید-۱۹ در کشورهایی که مطالعات در آنها به طور قابل توجهی منشأ گرفته است از تعداد موارد COVID-19 پیشی گرفته است. بنابراین، به نظر می رسد که ارتباط بین عفونت و ایجاد سندرم نفروتیک قوی تر از ارتباط بین واکسیناسیون و ایجاد سندرم نفروتیک باشد.
سوابق پزشکی
مشخص شده است که سندرمهای نفروتیک اغلب با سایر بیماریهای همراه، بهویژه با علت عفونی و بدخیمی همراه است. با این حال، در میان بیماران گزارش شده که پس از عفونت COVID-19 یا واکسیناسیون دچار سندرم نفروتیک شدهاند، نتوانستیم ارتباط واضحی بین عفونتهای مزمن یا سابقه سرطان پیدا کنیم. تنها ۶ نفر از بیماران سابقه عفونت مزمن را ثبت کرده بودند و هیچ دو بیمار یک نوع عفونت مزمن را نداشتند. مالهوترا و همکاران یک مورد از FSGS را در یک بیمار با سابقه شناخته شده HIV، یک عامل خطر شناخته شده برای FSGS گزارش کرد. عفونت HIV را می توان به عنوان یک عامل مخدوش کننده احتمالی در نظر گرفت زیرا این بیمار بدون توجه به عفونت COVID-19 در معرض خطر بیشتری قرار داشت. با این حال، اگر ارتباط بین COVID-19 و FSGS وجود داشته باشد، قابل قبول است که بیماران مبتلا به HIV که به COVID-19 مبتلا می شوند در معرض خطر بالایی از FSGS باشند، اما این ادعا به داده های قابل توجهی بیشتری برای اثبات نیاز دارد. علاوه بر این، تاریخچه هپاتیت مزمن B و C در میان بیماران مورد مطالعه که دچار FSGS شده بودند، یافت شد، اما این عفونت ها کمتر با FSGS مرتبط هستند.
پنج بیمار سابقه سرطان داشتند و تنها سرطانی که بیش از یک بار ظاهر شد سرطان پروستات بود. با این حال، هر سه بیمار بالای ۶۰ سال سن داشتند و در آن سن، تعداد زیادی از مردان به انواع با پیشرفت آرام سرطان پروستات مبتلا شدند . فقط در یک بیمار سابقه استفاده از NSAID گزارش شده بود . لازم به ذکر است که جزئیات تاریخچه پزشکی بسیاری از بیماران ممکن است به اندازه کافی برای توصیف چنین تاریخچه هایی حتی در صورت وجود آنها دقیق نبوده باشد. علاوه بر این، NSAID ها را می توان بدون نسخه خریداری کرد. بسیاری از موارد در بین بیماران بدون سابقه قبلی CKD گزارش شده است. با این حال، برخی از بیماران با کراتینین بالا در ابتدا به عنوان بیماران با سابقه CKD ثبت نشدند. پنج گزارش از سندرم نفروتیک در کلیه های پیوندی وجود دارد. ارتباط واقعی این یافته مشکوک است زیرا تعداد افراد دارای کلیه پیوندی در جمعیت نسبتاً کم است، بنابراین حتی ۵/۷۸ عدد بهطور نامتناسبی بزرگ به نظر میرسد. گزارش موردی از بیماران مبتلا به سندرم نفروتیک قبلی حذف شد. اما این معیار در همه سری مواردی که درج شد اعمال نشد و به همین دلیل ممکن است در برخی از بیماران عود رخ داده باشد.
به طور خلاصه، با توجه به دادههایی که تاکنون در مطالعات گزارش شده است، تعیین اینکه آیا جنبه خاصی از سابقه پزشکی فرد را مستعد ابتلا به سندرم نفروتیک در شرایط عفونت COVID-19 یا واکسیناسیون میکند، دشوار است. جزئیات ناکافی در گزارش سوابق پزشکی گذشته بر یافتهها تأثیر میگذارد و گزارشهای موردی و مجموعههای موردی دقیقتر در آینده مورد نیاز است تا تصویر واضحتری از هرگونه ارتباط احتمالی ارائه شود. امکان سنجی یک مطالعه مورد-شاهدی برای ارزیابی نسبت شانس برای هر یک از متغیرهای فوق الذکر به دلیل درک ناقص از شیوع واقعی شرایط مورد تردید است.
یافته های بالینی و مدیریت
سندرم نفروتیک با از دست دادن پروتئین در ادرار مشخص می شود که منجر به یافته های مشخصه ادم گسترده، انعقاد بیش از حد، افزایش چربی خون و سایر اختلالات متابولیک می شود. علائم معمول COVID-19 علائم تنفسی فوقانی و تحتانی است، اما اغلب اندام های دیگر را تحت تاثیر قرار می دهد. هر بیماری که باعث سرکوب سیستم ایمنی شود، فرد را مستعد ابتلا به عفونت های شدید، از جمله COVID-19 می کند. بنابراین، مهم است که مشخص شود آیا سندرم نفروتیک قبل یا بعد از شروع COVID-19 رخ داده است یا خیر، و مواردی را که ظن قوی وجود داشته باشد که سندرم نفروتیک قبل از شروع علائم مرتبط با COVID-19 وجود داشته باشد را حذف کردیم. در میان موارد گزارش شده، اکثر بیماران در عرض هفت روز دچار سندرم نفروتیک شدند. با این حال، تفسیر این عدد امر دشواری است، زیرا نقطه مشخصی وجود ندارد که افراد به دنبال مراقبت های پزشکی باشند یا آزمایش کووید-۱۹ انجام دهند، و چون برخی ممکن است زودتر مراجعه کنند و برخی دیگر نه، خطر سوگیری افزایش می یابد. علاوه بر این، موارد بسیاری در سه روز اول گزارش شد. ارزیابی احتمالاً دقیقتر این است که آن را بر اساس روز شروع علائم انجام دهیم، اما در آن صورت، یافتهها به یادآوری ذهنی علائم بستگی دارد و احتمال سوگیری یادآوری را افزایش میدهد. طولانی ترین فاصله بین دو تشخیص گزارش شده چهار ماه بود. یکی دیگر از مسائل احتمالی که تفسیر دادهها را پیچیده میکند، در این مورد، شکاف بین زمانی که فرآیند پاتوفیزیولوژیک در نهایت به سندرم نفروتیک منجر میشود و زمانی که میتوان یافتههای بالینی یا بیوشیمیایی را تشخیص داد، است. ممکن است در برخی موارد، محرک اولیه برای سندرم نفروتیک قبل از شروع COVID-19 رخ داده باشد. چنین یافتههایی میتوانند مواردی با شکاف بیشتر بین COVID-19 یا واکسیناسیون و ایجاد سندرم نفروتیک مرتبطتر کنند.
شایع ترین علامت اولیه سندرم نفروتیک شروع ادم بود. با این حال، چندین بیمار تنها زمانی شناسایی شدند که علیرغم هیچ شکایتی پروتئینوریک بودند. پروتئینوری اغلب شدید بود و میانگین آن تقریباً ۱۲ گرم در ۲۴ ساعت بود. علاوه بر این، برخی از بیماران با سطوح بالای کراتینین سرم و AKI به عنوان یافته های اولیه خود مراجعه کردند. لازم به ذکر است که در برخی از موارد، بیماران پس از بیوپسی، یافته هایی مطابق با نوعی سندرم نفروتیک داشتند، اما هرگز پروتئینوری با دامنه نفروتیک ایجاد نشد. شدت عفونت COVID-19 در بین موارد مورد مطالعه بسیار متفاوت بود و هیچ ارتباط واضحی بین سندرم نفروتیک و هر شدت خاصی از عفونت COVID-19 وجود نداشت. یکی از بیماران بر اثر عفونت فوت کرد که با نرخ مرگ و میر فرضی کووید-۱۹ بین ۱ تا ۲ درصد ارتباط دارد.
درمان محافظه کارانه برای سندرم نفروتیک شامل مهار سیستم رنین-آنژیوتانسین-آلدوسترون (RAAS) و دیورتیک ها است. استروئیدها برای درمان تهاجمی تر تجویز می شوند. با این حال، کورتیکواستروئیدها برای درمان بیماران مبتلا به پنومونی COVID-19 نیز استفاده می شود. در حالی که متیل پردنیزولون و پردنیزون معمولاً برای سندرم نفروتیک استفاده می شوند، دگزامتازون عمدتاً در موارد COVID-19 استفاده می شود. بیشترین کورتیکواستروئید گزارش شده در بین بیماران با هر دو بیماری پردنیزون بود، اگرچه دو مورد دیگر نیز گزارش شده بودند. نویسندگان تجویز استروئیدها را در بسیاری از موارد بدون مشخص کردن نوع استروئید گزارش کرده اند. هیچ ارتباط واضحی بین درمانهای اختصاصی COVID-19 و احتمال بهبودی کلیوی در این گروه از بیماران وجود ندارد، اگرچه گزارشدهی ناکافی میتواند نقش داشته باشد. گاهی اوقات از داروهای سرکوب کننده ایمنی دیگر نیز استفاده می شد. از نظر زمانی، COVID-19 با برخی از این عوامل (به عنوان مثال، هیدروکسی کلروکین) درمان شده است. بسیاری از بیماران بهبودی کامل یا نسبی در عملکرد کلیه را تجربه کردند. قابل ذکر است، افرادی که پس از عفونت دچار سندرم نفروتیک شدهاند، به نظر میرسد بیشتر احتمال دارد که از آسیب کلیوی باقیمانده رنج ببرند، از جمله، در موارد نادر، نیاز به همودیالیز در پایان دوره پیگیری. ۱۶ گزارش از این مساله وجود داشت و هر ۱۶ مورد به دنبال عفونت رخ داده است. نکته مهم، در ۶۲ مورد، عملکرد نهایی کلیه به صورت شفاهی یا با نشان دادن تغییر در کراتینین سرم توصیف شد. در ۲۳ مورد از این موارد، عملکرد کلیه ثابت ماند یا بدتر شد، در حالی که در بقیه موارد، بهبود یافت.
به طور خلاصه، تظاهرات بالینی و پیش آگهی بیماران مبتلا به سندرم نفروتیک در زمینه عفونت یا واکسیناسیون اخیر COVID-19 بسیار متفاوت است و تقریباً هر نوع سندرم نفروتیک می تواند توسط آنها ایجاد شود. به نظر می رسد شایع ترین شکل، فروپاشی گلومرولواسکلروز سگمنتال کانونی باشد، اما FSGS نیز یکی از شایع ترین علل سندرم نفروتیک در بزرگسالان است. علاوه بر این، زمان شروع و تظاهرات بالینی سندرم نفروتیک یکسان نبود. استروئیدها اغلب تجویز میشوند، و به نظر میرسد که اکثر پزشکان پردنیزون که کورتیکواستروئید انتخابی برای سندرم نفروتیک است را به دگزامتازون، استروئید انتخابی برای COVID-19 در زمانی که هر دو بیماری به طور همزمان رخ میدهند، ترجیح میدهند. گلومرولواسکلروز فوکال سگمنتال معمولاً پیش آگهی نسبتاً ضعیفی دارد، بنابراین ممکن است این درست باشد که موارد مرتبط با کووید-۱۹ یا واکسن خفیفتر هستند، زیرا در اکثر موارد گزارششده، بیماران بهبود نسبی یا کامل عملکرد کلیه اولیه خود را تجربه کردند.
محدودیت های مطالعه
این مطالعه دارای چندین محدودیت قابل توجه است. اولاً، اکثر مقالات یا گزارش موردی یا چکیده هستند. علیرغم اینکه هر دو تابع فرآیند ارزیابی کیفیت هستند اما جزئیات محدودی به خصوص در مورد تاریخچه بیمار وجود دارد. علاوه بر این، مقدار کلی داده در مورد موضوع کمیاب است و خطر سوگیری انتشار وجود دارد. با توجه به تصادفی بودن نسبی که در آن اطلاعات از هر مطالعه به دست می آید، بیشتر یافته ها فقط به صورت توصیفی قابل گزارش هستند که خطر سوگیری انتخاب را افزایش می دهد.
دستورالعمل های آینده
کمبود داده ها در این نوع مطالعه یکی از چالش های اصلی بوده است. موارد بیشتری برای درک بهتر بروز و عوامل مرتبط با ایجاد سندرم نفروتیک در بیماران مبتلا به COVID-19 یا پس از واکسیناسیون COVID-19 ضروری است. علاوه بر این، برای تعیین اینکه آیا سندرم نفروتیک میتواند به سایر بیماریها یا داروها نیز مرتبط باشد، به اطلاعات بیشتری نیاز دارد. هیچ دستورالعمل روشنی در مورد مناسب ترین درمان موجود نیست. بنابراین، یک کارآزمایی بالینی تصادفی شده با مقایسه پردنیزون و دگزامتازون در شرایط همزمان کووید-۱۹ و سندرم نفروتیک میتواند مفید باشد اما به دلیل نادر بودن چنین ارائه ای، احتمالاً یک مطالعه چند مرکزی ضروری است.
نتیجه گیری
هم عفونت COVID-19 و هم واکسیناسیون COVID-19 می توانند با سندرم نفروتیک مرتبط باشند که اغلب به صورت فروپاشی FSGS با پروتئینوری و ادم قابل توجه تظاهر می کند، اما انواع دیگری از سندرم نفروتیک و سایر تظاهرات بالینی گزارش شده است. هیچ ارتباط واضحی بین هیچیک از جنبههای سوابق پزشکی گذشته و ایجاد سندرم نفروتیک وجود ندارد، همچنین شدت کووید-۱۹ با این وضعیت مرتبط نبود. هنگامی که بیماران پس از عفونت یا واکسیناسیون با کووید-۱۹ دچار ادم، افزایش سطح کراتینین یا پروتئینوری قابل توجهی می شوند، سندرم نفروتیک باید در نظر گرفته شود و درمان در اسرع وقت آغاز شود زیرا به نظر می رسد پیش آگهی در افرادی که درمان به موقع دریافت می کنند مطلوب باشد. درمان با استروئیدها، در درجه اول پردنیزون، معمولاً علائم را بهبود بخشیده یا برطرف کرده است. به دلیل عدم یکنواختی در گزارش دهی داده ها در گزارش های موردی تجزیه و تحلیل شده، قبل از اینکه بتوان در مورد ارتباط های احتمالی نتیجه گیری قطعی کرد، به گزارش های موردی و کیس ریپورت سریال دقیق تر نیاز است.