یک مطالعه پیگیری طولی با استفاده از یک گروه نمونه از سراسر کشور
خلاصه
پسوریازیس یک بیماری شناخته شده با واسطه سیستم ایمنی است. پاتوفیزیولوژی آن شامل تاثیر بر عروق سیستمیک با واسطه ایمنی است که در مورد پاتوژنز کاهش شنوایی حسی عصبی ناگهانی (SSNHL) همخوانی دارد است. هدف از مطالعه ما بررسی اینکه آیا پسوریازیس بر شیوع SSNHL در همه گروههای سنی مطابق با سن، جنس، درآمد و منطقه محل سکونت تأثیر میگذارد یا خیر بود. نمونههای ما از جمعیت تحت پوشش بیمه سلامت کره از سال 2002 تا 2013 جمعآوری شد. یک گروه پسوریازیس مطابق با 1:4 (12864 نفر) و گروه کنترل (51456 نفر) انتخاب شدند. نسبت های خطر خام (ساده) و تعدیل شده (شاخص همبودی چارلسون) (HR) برای پسوریازیس و SSNHL با استفاده از مدل طبقه بندی شده کاکس مورد تجزیه و تحلیل قرار گرفت. بروز SSNHL در گروه پسوریازیس به طور قابل توجهی بیشتر از گروه کنترل بود (0.5٪ در مقابل 0.4٪، p = 0.004). بدین معنی که پسوریازیس خطر SSNHL را افزایش میدهد (HR = 1.44، فاصله اطمینان 95% (CI) = 1.09-1.90، p = 0.010). در تجزیه و تحلیل طبقه بندی، بروز SSNHL در گروه 30-59 ساله به طور قابل توجهی بالاتر از سایر گروه های SSNHL بود (HR تنظیم شده = 1.50، 95٪ CI = 1.06-2.12، p = 0.023). علاوه بر این، SSNHL در مردان مبتلا به پسوریازیس به طور قابل توجهی بیشتر رخ می دهد (HR تنظیم شده = 1.70، 95٪ CI = 1.17-2.49، P = 0.006). لذا پسوریازیس خطر ابتلا به SSNHL را افزایش میدهد و SSNHL در سنین 30 تا 59 سال و در مردان مبتلا به پسوریازیس شایعتر بود.
معرفی
کم شنوایی حسی عصبی ناگهانی (SSNHL) به عنوان کم شنوایی 30 دسی بل در سه فرکانس متوالی در ادیومتری تون خالص تعریف می شود که در عرض 72 ساعت رخ می دهد. بروز سالانه آن بین 5 تا 20 در 100000 نفر تخمین زده می شود. عوامل مختلفی مانند عفونت ویروسی و متابولیسم، خودایمنی و آسیب شناسی سیستم عصبی مرکزی به عنوان علت SSNHL گزارش شده است، اما اکثر موارد SSNHL ایدیوپاتیک در نظر گرفته می شوند. از نظر ایمونولوژیکی، اعتقاد بر این است که SSNHL در اثر برهمکنش بین آنتی بادی های در گردش و یک آنتی ژن در گوش داخلی، توسط سلول های T فعال ایجاد می شود. علاوه بر این، فعال شدن سیستم کمپلمان می تواند مکانیسم توجیه کننده آسیب گوش داخلی باشد. نشان داده شده است که درمان سرکوب کننده سیستم ایمنی و کورتیکواستروئیدها گزینه های درمانی موثری برای SSNHL هستند که ممکن است با پاتوفیزیولوژی با واسطه ایمنی مرتبط باشد. همانند کاهش شنوایی حسی عصبی با واسطه ایمنی، تشخیص SSNHL با علت با واسطه ایمنی به دلیل فقدان آزمایشها و نشانگرهای زیستی که بتواند علت ایمونولوژیک را تعریف کند، دشوار است. با این حال، گزارشهایی وجود دارد که آنتیبادیهایی مانند آنتیبادیهای ضد اندوتلیال، آنتیکاردیولیپین، آنتیبادیهای ضد بتا۲-گلیکوپروتئین ۱ و آنتیبادیهای پروتئین ضد شوک حرارتی-۷۰ در SSNHL و ایجاد SSNHL در بیماران مبتلا به لوپوس اریتماتوز سیستمیک (SLE) نقش دارند. پسوریازیس و گرانولوماتوز Wegener نیز از علت دیگر SSNHL با واسطه ایمنی هستند.
پسوریازیس یک بیماری التهابی مزمن با واسطه ایمنی است که به صورت علائم پوستی و سیستمیک ظاهر می شود. فعال سازی سلول های T helper (Th) -1 و -17 مکانیسم های ایمونولوژیکی معمولی هستند که باعث التهاب سیستمیک می شوند. این منجر به تشکیل واسطه های پیش التهابی می شود که منجر به اختلال عملکرد سلول های اندوتلیال و فعال شدن پلاکت ها می شود. بیماری های قلبی عروقی، دیابت شیرین و بدخیمی در بیماران مبتلا به پسوریازیس بیشتر دیده می شود. پسوریازیس احتمالاً با واسطههای التهابی مرتبط است که هنگام وقوع فرآیندهای التهابی سیستمیک تولید میشوند. چند مطالعه گزارش کرده اند که پسوریازیس همچنین می تواند با کاهش ناگهانی شنوایی همراه باشد زیرا هر دو بیماری ممکن است یک پاتوژنز التهابی با واسطه ایمنی مشترک داشته باشند.
پسوریازیس و SSNHL اغلب در درماتولوژی و گوش و حلق و بینی دیده می شوند، اما ارتباط آنها به ندرت به عنوان گزارش موردی علیرغم فرضیه پاتوفیزیولوژیک زمینه ای آن گزارش شده است. مطالعه کوهورت حاضر با هدف بررسی ارتباط پسوریازیس بر شیوع SSNHL با استفاده از یک نمونه کوهورت مبتنی بر جمعیت در مقیاس بزرگ در سراسر کشور انجام شد.
مواد و روشها
جمعیت مطالعه و جمع آوری داده ها
این مطالعه همگروهی از سراسر کشور بر اساس داده های بیمه سلامت کره – گروه نمونه کشوری (HIRA-NSC) بود. شرح مفصل این داده ها در مطالعات قبلی ما شرح داده شده است.
انتخاب شرکت کننده
از 1,125,691 مورد شرکتکنندگانی را وارد کردیم که با پسوریازیس تشخیص داده شده بودند (ICD-10: L40). از بین آنها، شرکتکنندگانی را انتخاب کردیم که تحت درمان برای پسوریازیس ≥2 بار قرار گرفته بودند (تعداد = 12921). بنابراین شرکت کنندگان تا 12 سال پیگیری شدند.
SSNHL با استفاده از کدهای ICD-10 (H912) تشخیص داده شد. ما شرکتکنندگانی را که تحت معاینه شنواییسنجی قرار گرفتهاند (کد ادعا: E6931-E6937, F6341-F6348) و با استروئیدها درمان شدهاند را وارد مطالعه کردیم. از سال 2002 تا 2013، 5244 بیمار SSNHL به دنبال مطالعات قبلی ما انتخاب شدند.
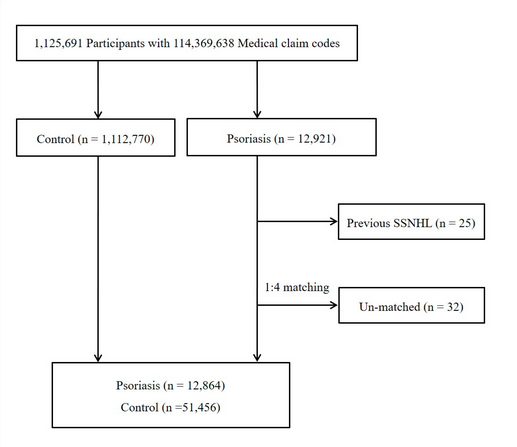
شرکتکنندگان پسوریازیس با شرکتکنندگان (گروه کنترل) که بین سالهای 2002 تا 2013 هرگز مبتلا به پسوریازیس تشخیص داده نشده بودند، با نسبت 1:4 همسان شدند. گروههای کنترل از جمعیت پایه (1112770=n) انتخاب شدند. بیماران و گروه شاهد از نظر سن، گروه، جنس، گروه درآمد و منطقه محل سکونت همسان شدند. برای جلوگیری از سوگیری انتخاب هنگام انتخاب شرکتکنندگان همسان، شرکتکنندگان گروه کنترل با استفاده از یک ترتیب اعداد تصادفی مرتب شده و از بالا به پایین انتخاب شدند. تاریخ شاخص به عنوان تاریخ تشخیص پسوریازیس تعیین شد. ما فرض کردیم که شرکتکنندگان کنترل همسان همزمان با شرکتکنندگان پسوریازیس که با آنها همسان شده بودند درگیر بودند (تاریخ شاخص). بنابراین، هر بیمار که قبل از تاریخ شاخص فوت کرده بود از گروه کنترل حذف شد. در هر دو گروه پسوریازیس و کنترل، افرادی که سابقه SSNHL قبل از تاریخ شاخص داشتند از مطالعه خارج شدند. در گروه پسوریازیس 25 شرکت کننده از مطالعه حذف شدند. اعضای گروه پسوریازیس که نتوانستیم شرکتکنندگان همسان کافی را برای آنها شناسایی کنیم، حذف شدند (32 نفر). در نهایت، تطابق 1:4 منجر به وارد شدن 12864 شرکت کننده در گروه پسوریازیس و 51456 شرکت کننده در گروه کنترل شد (شکل 1).
متغیرها
متغیرهای گروه سنی، جنس، درآمد و منطقه محل سکونت در پی مطالعات قبلی ما تعیین شدند. گروه های سنی در قالب 0-4، 5-9، 10-14… و 85+ سال طبقه بندی شدند. شاخص (CCI) برای 17 بیماری همراه به عنوان متغیر پیوسته (0 (بدون همبودی) تا 29 (چند بیماری همراه) استفاده شد.
تجزیه و تحلیل های آماری
برای مقایسه میزان ویژگی های عمومی بین گروه پسوریازیس و کنترل از آزمون کای دو استفاده شد.
برای تجزیه و تحلیل نسبت خطر پسوریازیس در SSNHL، از مدل کاکس طبقه بندی شده استفاده شد. در این تحلیل از مدل های خام (ساده) و تعدیل شده (CCI) استفاده شد. در این تحلیل، سن، جنس، درآمد و منطقه سکونت را طبقه بندی کردیم.
برای تجزیه و تحلیل زیرگروه، شرکت کنندگان را بر اساس سن و جنس (0-29 سال، 30-59 سال، 60+ سال؛ مرد و زن) تقسیم کردیم.
تجزیه و تحلیل دو دنباله انجام شد و مقادیر P کمتر از 0.05 معنی دار در نظر گرفته شد. نتایج با استفاده از SPSS نسخه 21.0 (IBM, Armonk, NY, USA) مورد تجزیه و تحلیل آماری قرار گرفت.
در دسترس بودن داده ها و مواد
انتشار داده ها توسط محقق شرعاً مجاز نمی باشد. همه داده ها از پایگاه داده خدمات اشتراک بیمه سلامت ملی (NHISS) https://nhiss.nhis.or.kr/ NHISS استخراج شد. این داده ها را برای هر محققی که تضمین می دهد با صرف مقداری هزینه از اخلاق تحقیق پیروی کند، در دسترس است.
نتایج
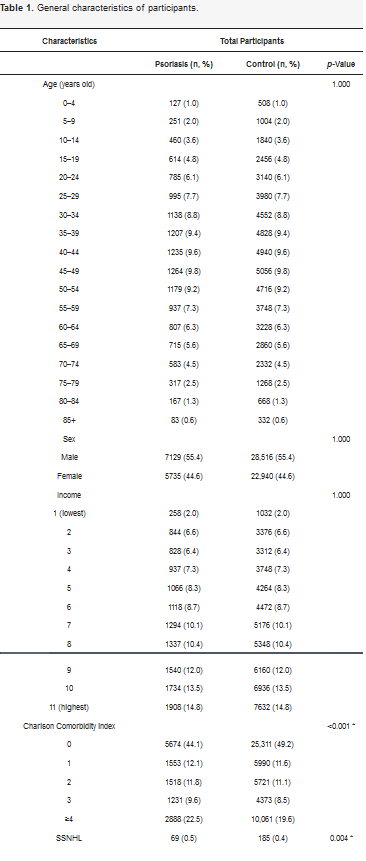
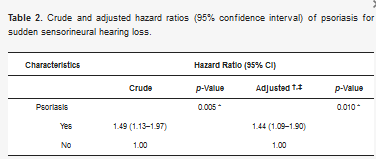
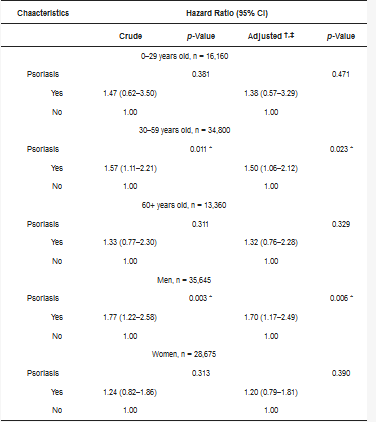
توزیع سن، جنس، سطح درآمد و منطقه محل سکونت بین گروه پسوریازیس و کنترل قابل مقایسه بود (جدول 1). این مطالعه شامل 12864 بیمار در گروه پسوریازیس و 51456 شرکت کننده همسان در گروه کنترل بود که چهار برابر این تعداد در گروه پسوریازیس بود. نسبت جنسی برای گروه پسوریازیس 55.4٪ (n = 7129) مرد و 44.6٪ (n = 5735) زن بود. همین نسبت برای گروه کنترل برقرار شد. نسبت بیماران در گروه پسوریازیس که در مناطق شهری زندگی می کردند 47.8٪ (6146 = n) بود در حالی که 52.2٪ (n = 6718) در مناطق روستایی زندگی می کردند. میزان SSNHL در گروه پسوریازیس 0.54% (69=n) و در گروه کنترل 0.36% (185=n) بود که در گروه پسوریازیس به طور قابل توجهی بیشتر بود (0.004=p). نسبت خطر خام و تنظیم شده (HR) به ترتیب 1.49 (95% CI = 1.13-1.97، p = 0.005) و 1.44 (95% CI = 1.09-1.90، p = 0.010) بود (جدول 2). تجزیه و تحلیل زیرگروهی نشان داد که HR تنظیم شده SSNHL در افراد 30 تا 59 ساله در مقایسه با گروه کنترل بالا بود (HR تنظیم شده 1.44، 95% CI = 1.06-2.12، p = 0.023) (جدول 3) . علاوه بر این، خطر SSNHL در مردان مبتلا به پسوریازیس حتی پس از تنظیم عوامل مخدوش کننده (HR = 1.70، 95% CI = 1.17-2.49، p = 0.006) افزایش یافت (جدول 3).
بحث
طی این مطالعه مشخص شد که پسوریازیس خطر SSNHL را در این گروه با پیگیری 12 ساله از سال 2002 تا 2013 افزایش میدهد. پسوریازیس به طور قابل توجهی خطر SSNHL را در میانسالان (30 تا 59 سال) نیز و گروه مرد در این گروه نمونه افزایش داد که با جنسیت، درآمد و منطقه مطابقت داشتند.
در یک مطالعه مشابه با استفاده از داده های همگروهی ملی در تایوان، بروز SSNHL در گروه پسوریازیس به طور قابل توجهی بیشتر از گروه کنترل بود. علاوه بر این، بروز SSNHL در بین بیماران پسوریازیس در سنین 35 تا 49 سال و افراد مسن تر از 65 سال به طور قابل توجهی بالاتر بود. اگرچه دادههای مربوط به تایوان دارای طبقهبندی سنی کمی متفاوت با این گروه بود، اما مطالعات مشابه بودند به این دلیل که هر دو میزان بروز SSNHL را در گروه میانسالی (30 تا 59 سال) و گروه سالمندی به طور قابلتوجهی بالاتر نشان دادند. ین و همکاران تفاوت معنی داری در بروز SSNHL در همه جنس های گروه پسوریازیس در مقایسه با گروه کنترل گزارش کردند. با این حال، در این مطالعه، شرکت کنندگان را با گروه بندی سن و جنسیت مورد تجزیه و تحلیل قرار دادیم. بروز SSNHL در زنان مبتلا به پسوریازیس در تمام سنین بالاتر از گروه شاهد نبود. تنها در گروه های سنی فوق (30 تا 59 سال) و مردان مبتلا به پسوریازیس به طور قابل توجهی بیشتر بود. اگرچه بیماری های خودایمنی مانند پسوریازیس در زنان بیشتر رخ می دهد، اما قابل توجه است که در این مطالعه بروز SSNHL در مردان بالای 30 سال بیشتر بود. علاوه بر این، اگرچه تعیین دقیق دلیل چنین نتیجه ای دشوار است، اما عواملی مانند تفاوت در ترکیب جمعیت بر اساس گروه سنی، نسبت جنسیتی و میزان استفاده از خدمات پزشکی بر اساس سن در کره جنوبی ممکن است بر آن تأثیر بگذارد. در مطالعه بعدی، بررسی ارتباط پاتوفیزیولوژیک با استفاده از این نتایج اپیدمیولوژیک ضروری است.
یکی از علل ایمونولوژیک SSNHL، اختلال در تغذیه میکروواسکولار حلزون گوش است که مشخص شده است که توسط اتوآنتی بادی هایی ایجاد می شود که باعث ایجاد شرایط ترومبوتیک در عروق لابیرنتی می شود. در پسوریازیس، التهاب عروقی سیستمیک توسط اینترلوکین (IL) -6، IL-12، IL-23، تولید فاکتور نکروز تومور (TNF) -α و استرس اکسیداتیو ایجاد می شود که باعث ترومبوز در عروق و اختلال در تنظیم چربی می شود. این دو بیماری جنبه های ایمونولوژیکی مشترک دارند اما تحقیقات کمی در مورد رابطه بین عوامل ایمنی و ایجاد این بیماری ها وجود دارد. لین و همکاران بروز SSNHL در بیماران SLE را با استفاده از دادههای همگروهی سراسری تجزیه و تحلیل کردند. آنها دریافتند که SLE که مانند پسوریازیس یک بیماری خودایمنی است نیز به طور قابل توجهی با افزایش بروز SSNHL مرتبط است و بروز SSNHL در افراد جوان (0 تا 34 سال) به طور قابل توجهی بیشتر از افراد میانسال و مسن است. علاوه بر این، بروز SSNHL در زنان به طور قابل توجهی بیشتر از گروه کنترل بود، و شروع SSNHL 1-3 سال و 3-5 سال پس از تشخیص SLE در مقایسه با کمتر از یک سال و بیش از 5 سال پس از تشخیص بیشتر بود. دادههای مقطعی از بانک بیولوژیک بریتانیا نشان میدهد که بیماری منیر بر بروز بیماریهای خودایمنی مختلف از جمله پسوریازیس تأثیر میگذارد. فرجو و همکاران نشان دادند که لوکوس PSORC1 و واریانت آللی rs4947296، هر دو در 6p21.33 واقع شده اند،که با تنظیم بیان ژن و تنظیم ترجمه NF-kB در القا ضعیف آپوپتوز/Fn14 مانند TNF، التهاب سد لابیرنت خون و کیسه اندولنفاتیک را ایجاد می کنند.
در پسوریازیس، سیتوکین های پیش التهابی مانند فاکتور نکروز تومور آلفا (TNF-α) و اینترلوکین (IL)-6 باعث ایجاد اختلال در عملکرد اندوتلیال می شوند و در نتیجه خطر بیماری قلبی عروقی و بروز بیماری ایسکمیک مغزی را افزایش می دهند. علاوه بر این، این سیتوکین ها می توانند با تحریک محور هیپوتالاموس-هیپوفیز، چاقی مرکزی و مقاومت به انسولین را القا کنند. مطالعات اخیر نشان داده است که پسوریازیس با میگرن مرتبط است، زیرا اختلال عملکرد اندوتلیال ناشی از افزایش TNF منجر به اختلال عروقی می شود . چو و همکاران گزارش دادند که میگرن یک عامل خطر برای SSNHL است، که نتیجه ای است که می تواند نشان دهد که سایتوکاین های پیش التهابی می توانند با رابطه بالقوه بین پسوریازیس و SSNHL مرتبط باشند. علاوه بر این، پسوریازیس به دلیل اختلالات ایمنی با واسطه Th 1 با رینوسینوزیت مزمن (CRS) بدون پولیپ بینی (NP) همراه است و نسبت خطر CRS بدون NP در بیماران پسوریازیس 2.01 (95% CI = 1.54-2.62) بود.
از آنجایی که SSNHL به طور بالقوه یک بیماری با واسطه ایمنی است، چندین مطالعه تلاش کرده اند تا ارتباطی بین آن و یک بیماری خودایمنی تثبیت شده پیدا کنند. با این حال، از آنجایی که این مساله نادر است که هر دو بیماری همزمان یا در مدت زمان کوتاهی رخ دهند، محققان با مشکل پیگیری بیماران برای دوره های طولانی مواجه هستند که ممکن است محدودیت این نوع مطالعات باشد. اخیراً، microRNA، جهش ژنی و تجزیه و تحلیل پلی مورفیسم برای ارتباط با کاهش شنوایی در پسوریازیس بررسی شده است. 9 میکرو RNA مربوط به کم شنوایی و 12 ژن هدف با تجزیه و تحلیل بیوانفورماتیک از نمونه های پلاسمایی بیماران پسوریازیس شناسایی شدند . علاوه بر این، جهش در ژن بتا-2 (Cx26) بیان شده در سلول های اندام کورتی و کاهش تنظیم Cx26 در بیماران پسوریازیس مشاهده شد. کاهش Cx26 باعث مرگ سلولی سلولهای مویی و استریا عروقی در حلزون میشود، اتصالات شکاف سلولهای پوست را مختل میکند و میتواند با تظاهرات پوستی مختلف پسوریازیس مرتبط باشد.
این مطالعه در مقایسه با سایر مطالعات دارای مزایای متعددی است. داده های مورد استفاده در تجزیه و تحلیل از یک کوهورت در سراسر کشور بدست آمده است و مهمترین مزیت آن این است که پایگاه داده با تطبیق بیماران و موارد کنترل از نظر سن، جنس، منطقه سکونت و عوامل درآمد ساخته شده است. کنترل بسیاری از عوامل مخدوش کننده در تجزیه و تحلیل بروز SSNHL به عنوان یک متغیر وابسته ممکن است قابلیت اطمینان نتایج را افزایش داده باشد. یک مزیت اضافی این است که معیارهای ورود برای بیماران SSNHL واضح بود. اگرچه مطالعات همگروهی در سراسر کشور این مزیت را دارند که میتوانند تعداد زیادی از افراد را شامل شوند، اما اگر متغیر مورد تجزیه و تحلیل علامتی باشد که یک موجودیت کل برای بیماری نیست، سوگیری یادآوری ممکن است رخ دهد. علاوه بر این، ایجاد معیارهای ورود و به دست آوردن نتایج قابل اعتماد دشوار است. در مطالعه حاضر، شواهد SSNHL از سوابق پزشکی بیمار و سیستم داده HIRA به دست آمد. ما از شواهد تشخیصی با استفاده از نتایج آزمایش شنواییسنجی تون خالص و نسخهها به عنوان معیارهای ورود، که از سوگیری یادآوری جلوگیری میکرد، استفاده کردیم. از آنجایی که دادههای HIRA برای همه افراد در کشور نگهداری میشود، موضوعاتی که در تجزیه و تحلیل قرار گرفتند در طول پیگیری نادیده گرفته نشدند. علاوه بر این، از آنجایی که زمان تشخیص واضح بود، اثر مخدوش کننده ناشی از سابقه SSNHL قبل از شروع پسوریازیس به حداقل رسید.
اگرچه ما متوجه شدیم که پسوریازیس بروز SSNHL را افزایش می دهد، اما چند نقطه ضعف در تحقیقات ما وجود دارد. ما نمیتوانستیم میزان اختلال شنوایی را در زمان تشخیص تعیین کنیم، زیرا آستانههای شنوایی را در ادیوگرام برای همه افراد دریافت نکردیم. بهعلاوه، شناسایی دادههای سلامت عمومی برای بیماران فردی، مانند قد، وزن، سیگار کشیدن، نوشیدن، و سابقه قرار گرفتن در معرض صدا در سیستم داده HIRA دشوار است. علل مختلفی برای SSNHL وجود دارد مانند عفونت، ضربه به سر، بیماری های خود ایمنی، داروها، گردش خون و اختلالات عصبی. اما در داده های ارائه شده به محققین نمی توان اطلاعات توصیفی را که بر اساس عوامل مذکور گروه بندی میشوند را، به دست آورد. اطلاعات خاصی در مورد ضایعات پوستی، تیتر اتوآنتی بادی و تظاهرات سیستمیک در بیماران مبتلا به پسوریازیس نیز در دسترس نیست. بنابراین، مطالعات آینده باید تعیین کنند که آیا SSNHL با عواملی که نشان دهنده فعالیت بیماری پسوریازیس هستند و اینکه دقیقا کدام عوامل ایجاد کننده SSNHL با پسوریازیس ارتباط دارد ، مرتبط است یا خیر. علاوه بر این، تمام مطالعات در مورد ارتباط بین SSNHL و پسوریازیس در سراسر کره جنوبی، مطالعات مبتنی بر جمعیت در جمعیت های نژاد آسیایی بوده است، و هیچ مطالعه اپیدمیولوژیک در جمعیت فرزندان اروپایی در دسترس نیست. بر اساس نتایج این مطالعه، می توان شواهدی برای ارتباط بین این دو بیماری با گسترش آن به یک گروه سراسری با هدف قرار دادن نژادها و کشورهای مختلف ایجاد کرد.
نتایج نشان می دهد که پزشکانی که مسئول بیماران مبتلا به پسوریازیس هستند باید در طول دوره پیگیری از اختلال شنوایی آگاه باشند. علاوه بر این، از آنجا که SSNHL یک اورژانس گوش است، تشخیص زودهنگام مهم است. بنابراین، بیماران مبتلا به پسوریازیس باید از احتمال بروز نارسایی شنوایی ناگهانی مطلع شوند و باید از درمان اولیه مناسب آگاه باشند.

