۱. معرفی
تحقیقات قبلی قبلاً گزارش دادهاند که عفونتهای ویروسی ممکن است دلیل بالقوه AMI باشند، بهویژه زمانی که دستگاه تنفسی درگیر باشد. در این راستا، تجزیه و تحلیل های اخیر نشان داده است که COVID-19 با افزایش خطر انفارکتوس حاد میوکارد (AMI) مرتبط است. با این حال، مطالعات اخیر که رابطه بین AMI و عفونت SARS-CoV-2 را بررسی میکنند، عمدتاً بر مکانیسمهای پاتوفیزیولوژیکی بالقوه زیربنای این رابطه متمرکز شدهاند. در مقابل، دادههای مربوط به خطر ابتلا به AMI بهعنوان یک پیامد پس از حاد COVID-19 کم است. هدف مقاله پیش رو ارزیابی خطر بروز AMI در بیماران بهبودیافته COVID-19 با انجام یک بررسی سیستماتیک و متاآنالیز از داده های موجود است.
۲. مواد و روش ها
۲.۱. طراحی مطالعه
این مطالعه از دستورالعملهای مربوط به بررسیهای سیستماتیک و متاآنالیز (PRISMA) پیروی کرد (فایل تکمیلی ۱). دادهها با جستجوی MEDLINE و Scopus برای همه مطالعات منتشر شده تا تاریخ ۱ سپتامبر ۲۰۲۲ و گزارش خطر وقوع AMI در بیماران بهبود یافته COVID-19 با تشخیص بین ۴ ماه (حداقل طول مدت پیگیری بررسیهای تجدیدنظر شده) و حداکثر ۱۲ ماه پس از ترخیص (حداکثر طول مدت پیگیری مطالعات تجدید نظر شده) به دست آمد. در دستنوشتههای اصلاحشده، این گروه از بیماران با گروههای معاصر به عنوان افرادی که عفونت SARS-CoV-2 را تجربه نکردند و در همان دوره پیگیری، AMI ایجاد کردند، مقایسه شدند.
۲.۲. استخراج داده ها و ارزیابی کیفیت
انتخاب مطالعات گنجانده شده در تحلیل ما به طور مستقل توسط دو نویسنده (M.Z.، C.B.) به صورت Blind انجام شد. هر گونه اختلاف در انتخاب مطالعه با مشورت با نویسنده سوم (G.R.) حل شد. عبارات MeSH زیر برای جستجو استفاده شد: “انفارکتوس حاد میوکارد” و “عواقب COVID-19” یا “انفارکتوس حاد میوکارد” و “COVID-19”. علاوه بر این، ما کتاب ها را برای منابع اضافی جستجو کردیم.
به طور خاص، معیارهای ورود عبارت بودند از: (۱) مطالعاتی که افراد مبتلا به عفونت COVID-19 تایید شده قبلی را ثبت نام کردند (۲) ارائه نسبت خطر (HR) و فاصله اطمینان نسبی ۹۵٪ (CI) برای خطر وقوع AMI پس از عفونت در مقایسه با زمان معاصر. گروه های کنترل در مقابل، گزارشهای موردی، مقالات مروری، چکیدهها، سرمقالهها/نامهها و Case Series با کمتر از ۱۰ شرکتکننده حذف شدند. استخراج داده ها به طور مستقل توسط دو نویسنده (M.Z.، G.R) انجام شد. برای تمام تحقیقات بررسی شده، تعداد بیماران ثبت نام شده، میانگین سن، جنسیت، شیوع بیماری های قلبی عروقی مانند فشار خون شریانی (HT)، دیابت شیرین (DM)، بیماری انسدادی مزمن ریه (COPD)، بیماری مزمن کلیه (CKD)، چاقی، نارسایی قلبی از قبل موجود (HF)، بیماری عروق مغزی و طول مدت پیگیری را استخراج کردیم. کیفیت مطالعات وارد شده با استفاده از مقیاس ارزیابی کیفیت نیوکاسل-اتاوا (NOS) درجهبندی شد.
۲.۳. سنتز و تجزیه و تحلیل داده ها
متغیرهای پیوسته به صورت میانگین و متغیرهای طبقه بندی به صورت اعداد و درصدهای نسبی ارائه شدند. بروز تجمعی AMI (n/N)، که به عنوان نسبت بین بیمارانی که این رویداد را در طول دوره پیگیری (n) تجربه کردهاند و تعداد بیماران ثبتنام شده در هر مطالعه (N) تعریف میشود در نظر گرفته میشود و با استفاده از یک مدل اثرات تصادفی ادغام شدند و با فاصله اطمینان ۹۵% مربوطه (CI) ارائه شد. برعکس، برای تخمین خطر AMI در طی یک سال پس از عفونت، نسبت خطر (HR) با فاصله اطمینان ۹۵ درصد (CI) با استفاده از یک اثر تصادفی ادغام شد. تحلیلهای حساسیت از پیش تعریفشده (تحلیل ترک یکنفره) با حذف یک مطالعه در آن زمان انجام شد تا پایداری نتایج ما ارزیابی شود. ناهمگونی آماری بین گروه ها با استفاده از آمار هیگینز I2 اندازه گیری شد. وجود سوگیری انتشار بالقوه با بازرسی بصری طرح قیف تأیید شد. به دلیل تعداد کم مطالعات وارد شده (<10)، سوگیری مطالعات کوچک مورد بررسی قرار نگرفت زیرا تجزیه و تحلیل ما برای تشخیص چنین سوگیری ضعیف بود. برای ارزیابی بیشتر تأثیر عوامل مخدوش کننده بالقوه ، یک تحلیل متارگرسیون نیز انجام شد. تمام متاآنالیزها با استفاده از نرم افزار فراآنالیز جامع نسخه ۳ (Biostat، ایالات متحده آمریکا) انجام شد.
۳. نتایج
۳.۱. نتایج جستجو و مطالعات شامل
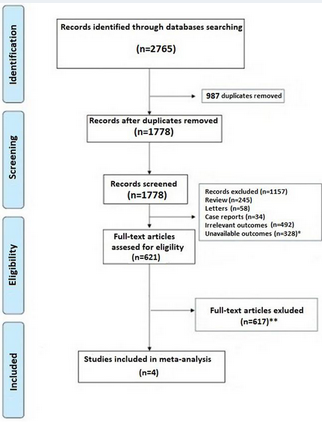
در مجموع ۲۷۶۵ مقاله با استفاده از استراتژی جستجوی ما به دست آمد. پس از حذف موارد تکراری و غربالگری اولیه، ۶۲۱ مقاله متن کامل از نظر واجد شرایط بودن ارزیابی شدند، ۶۱۷ مطالعه به دلیل عدم رعایت معیارهای ورود حذف شدند، و ۴ تحقیق دارای معیارهای ورود بودند (شکل ۱).
۳.۲. ویژگی های جمعیت و ارزیابی کیفیت
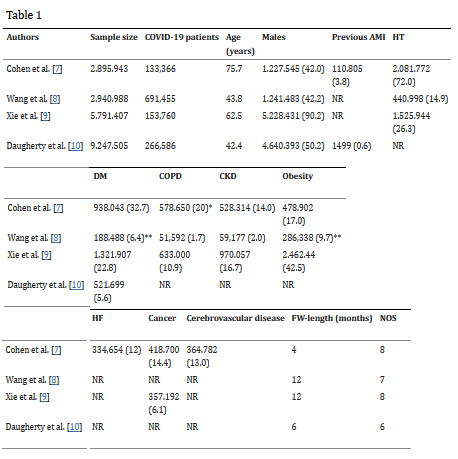
به طور کلی، ۲۰،۸۷۵،۸۴۳ بیمار (میانگین سن ۵۶.۱ سال، ۵۹.۱٪ مرد در این تجزیه و تحلیل قرار گرفتند). از میان آنها ۱۲۴۵۱۵۷ مورد ابتلا به کووید-۱۹ را تایید کرده بودند. مشخصات کلی مطالعات وارد شده در جدول ۱ نشان داده شده است. اگرچه ویژگی های جمعیت شناختی و بیماری های همراه به طور سیستماتیک در تمام تحقیقات ثبت نشد، گروه ها عمدتاً شامل بیماران میانسال بودند. میانگین طول مدت پیگیری ۸.۵ ماه و بین ۴ تا ۱۲ ماه بود. بررسیهای بازبینیشده، وقوع AMI را با غربالگری سوابق پزشکی بیماران ثبتنامشده با استفاده از کدهای I21 و I22 ویرایش ۱۰ طبقهبندی بینالمللی بیماریها (ICD-10) شناسایی کرد. ارزیابی کیفیت نشان داد که تمامی مطالعات بر اساس مقیاس NOS از کیفیت متوسط تا بالا برخوردار بودند.
۳.۳. تلفیق بروز انفارکتوس حاد میوکارد پس از ترخیص
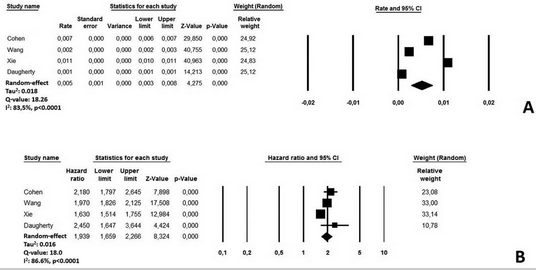
میزان تجمعی AMI پس از ترخیص در بیماران بهبود یافته کووید-۱۹ بین ۰.۱ تا ۱.۱ درصد در میان مطالعات بررسی شده بود. یک مدل اثر تصادفی بروز تلفیقی از AMI پس از COVID-19 را در ۰.۵٪ موارد نشان داد (۹۵٪ CI: 0.3-0.0.8، I2: 99.8٪) (شکل ۲، پانل A). تجزیه و تحلیل حساسیت میزان بروز ترکیبی را نشان داد که از نظر آماری معنیدار باقی ماند که در محدوده ۰.۳% موارد (۹۵% CI: 0.1-0.5، I2: 99.8%) تا ۰.۷% موارد (۹۵% CI: 0.2 تا ۱.۲؛ I2: 99.3%) بود. نشان داده شدهاست که هیچ تحقیقی تأثیر نامناسبی بر نتیجه مطالعه نداشته است. بازرسی بصری طرح قیف در فایل تکمیلی ۲، پانل A ارائه شده است. با این حال، ارزیابی بصری نمودار قیف به دلیل تعداد محدود مطالعاتی که در آنالیز گنجانده شده است، نمی تواند وجود عدم تقارن را تضمین کند. برعکس، همیشه یک مدل اثر تصادفی بروز تلفیقی AMI را در بین گروههای کنترل معاصر در ۰.۲ موارد نشان داد (۹۵% فاصله اطمینان (CI: 0.18-0.23، I2: 99.7%). همچنین در این مورد، تجزیه و تحلیل حساسیت نتایج را تایید کرد.
۳.۴. خطر طولانی مدت انفارکتوس حاد میوکارد
پس از میانگین پیگیری ۸.۵ ماهه، بیماران مبتلا به کووید-۱۹ بهبودیافته خطر بیشتری برای بروز AMI داشتند (HR: 1.93، ۹۵% فاصله اطمینان (CI: 1.65-2.26، p <0.0001، I2 = 83.5%) (شکل ۲، پانل ب).
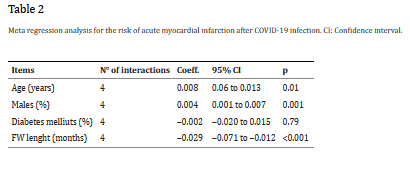
همچنین در این مورد، ارزیابی بصری نمودار به دلیل تعداد محدود مطالعاتی که در تجزیه و تحلیل بر اساس معیارها(فایل تکمیلی ۴) در نظر گرفته شده است، نمی تواند در مورد وجود عدم تقارن اطمینان حاصل کند در حالی که تجزیه و تحلیل حساسیت گزارش نتایج به دست آمده را تأیید می کند. HR در محدوده ۱.۸۸ (۹۵% CI: 1.60-2.21، p <0.0001) و ۲.۰۰ (۹۵% CI؛ ۱.۸۷-۲.۱۳، p <0.0001)، که به این معنی است که نتایج به دست آمده توسط هیچ مطالعه منفرد هدایت نشده است. تجزیه و تحلیل متارگرسیون رابطه مستقیم معنیداری را بین خطر ابتلا به AMI و سن (۰۱/۰=p) و جنس مذکر به عنوان تعدیلکننده نشان داد، در حالی که ارتباط غیرمستقیم زمانی مشاهده شد که طول مدت پیگیری (۰۰۱/0p<) به عنوان تعدیلکننده اتخاذ شد. متغیرها در (جدول ۲) نشان داده شده است.
۴. بحث
یافته های ما، بر اساس جمعیت بزرگ بیش از ۲۰ میلیون نفر، نشان داد که AMI در حدود ۰.۵٪ از بیماران بهبود یافته COVID-19 در طول دوره پیگیری رخ داده است. علاوه بر این، پس از بهبودی COVID-19، بازماندگان تقریباً ۹۳ درصد بیش از حد در خطر ابتلا به AMI بودند که با طول مدت پیگیری رابطه معکوس داشت. به طور قابلتوجه، بروز و خطر ابتلا به AMI در بیماران بهبودیافته کووید-۱۹ در مقایسه با گروه کنترل در یک میانگین پیگیری ۸.۵ ماهه بالاتر بود. در مقابل، خطر ابتلا به AMI پس از ترخیص از بیمارستان در مقایسه با سایر شرایط التهابی دستگاه تنفسی، مانند ذات الریه، کمتر بود. با این حال، نمیتوانیم این موضوع را رد کنیم که AMI از دست رفته ممکن است به ریسک بالای مشاهدهشده در تجزیه و تحلیل ما کمک کرده باشد، و کیس های AMI ی مورد استفاد با بازبینی کدهای ICD در جمعیت مورد تجزیه و تحلیل شناسایی شدهاند. علاوه بر این، این عدم قطعیت با ناهمگونی آماری بالای مشاهده شده منعکس می شود. تجزیه و تحلیل متارگرسیون به تعریف این ناهمگونی بالا کمک کرد و نشان داد که خطر AMI به طور مستقیم با افزایش سن افزایش می یابد، همانطور که قبلاً در افرادی از جمعیت عمومی و همچنین در مردان نیز گزارش شده بوده است. با این حال، این نیز درست است که مقایسه نرخ براساس جنسیت به شدت به محدوده سنی جمعیت مورد مطالعه بستگی دارد اما زمانی که میزان مرگ و میر ناشی از عللی غیر از بیماری مورد نظر بالا باشد، نرخ بروز بیماری به دلیل وجود خطرات رقیب، به طور کلی در تجزیه و تحلیل Kaplan-Meier بیش از حد تخمین زده می شود. علاوه بر این، نتایج ما نشان داد که خطر AMI فقط به مرحله حاد COVID-19 محدود نمی شود، بلکه در مرحله اولیه پس از بهبودی نیز وجود دارد. متأسفانه، مطالعات تجدیدنظر شده به طور سیستماتیک دادههای مربوط به عوامل خطر بالقوه برای AMI، و همچنین تظاهرات بالینی و نوع آنها (به عنوان مثال، با بالا رفتن یا نبودن قطعه ST) را گزارش نکردند. علاوه بر این، هیچ اطلاعاتی در مورد میزان مرگ و میر مرتبط با AMI در افراد بهبودیافته COVID-19 و همچنین برای افراد کنترل ارائه نشده است. بروز AMI مشاهده شده در بیماران بهبود یافته COVID-19 حدود ۳.۵ مورد AMI در هر ۱۰۰۰ نفر بود. با این حال، انجام یک مقایسه واقعی با سوابق اپیدمیولوژیک فعلی مشتق شده از جمعیت عمومی دشوار است، زیرا این داده ها به طور کلی بر اساس ۱۰۰۰ نفر در سال است در حالی که نتایج ما را نمی توان به همان دوره ارجاع داد. با این حال، یک تحقیق قبلی که بروز AMI شناخته شده و ناشناخته را در افراد بالای ۵۵ سال گزارش کرده بود، نشان داد که طی یک پیگیری متوسط ۶.۴ سال، میزان بروز این رویداد ۵.۰ در هر ۱۰۰۰ نفر سال بود. این نتیجه در مقایسه با نتایج مشاهده شده در گروه ما از بیماران بهبودیافته COVID-19 که احتمالاً ویژگی های جمعیتی مشابهی داشتند، بالاتر به نظر می رسد. احتمالاً، ما میزان بروز AMI را هم در بیماران بهبودیافته COVID-19 و هم در گروههای کنترل دستکم گرفتهایم. در واقع، تحقیقات قبلی به طور گسترده میزان بروز کمتر سندرمهای حاد کرونری را در طول همهگیری COVID-19 گزارش کردهاند. علاوه بر این، ما نمیتوانیم این نکته را رد کنیم که برخی از AMIها به عنوان آسیبهای قلبی عروقی مرتبط با عفونت حاد تشخیص داده نشده یا به اشتباه تفسیر شدهاند.
قبل از همهگیری COVID-19، تجزیه و تحلیلهای مختلف به خطر ابتلا به AMI پس از عفونت اشاره کردند. در این راستا، توضیح داده شده است که خطر ابتلا به AMI در عرض چند ماه پس از رفع عفونت به حالت اولیه باز می گردد و به نظر می رسد خطر حوادث حاد در بین بیماران مبتلا به بیماری شدیدتر بارزتر است .متأسفانه، دادههای مربوط به شدت عفونت SARS-CoV-2 بهطور سیستماتیک توسط مطالعات بررسیشده جمعآوری نشد که این امر یک تحلیل فرعی خاص را غیرممکن میسازد. از نقطه نظر پاتوفیزیولوژیک، گزارش شده است که بیماران COVID-19 ممکن است ریزش طولانی مدت ریبونوکلئیک اسید (RNA) SARS-CoV-2 را تا ۸۳ روز در دستگاه تنفسی فوقانی، همراه با لود بالای RNA ویروسی نشان دهند. علاوه بر این، در بیماران مبتلا و همچنین در بیماران بهبودیافته، حالت هیپرانعقادی پایدار ممکن است خطر ترومبوز عروق کرونر را در محلهای از هم گسیختگی پلاک افزایش دهد . بدون شک، سایر عوامل همزمان ممکن است به ترومبوز عروق کرونر کمک کنند، مانند تولید تلههای خارج سلولی نوتروفیلی (NETs) از داخل پلاک و نوتروفیلهای در گردش، افزایش فعالیت پلاکتی، اختلال در فیبرینولیز و به طور کلی کاهش عملکرد ضد انعقادی اندوتلیوم. اگرچه مطالعات اختصاصی بیشتری برای تعیین دقیق بروز AMI پس از عفونت COVID-19 مورد نیاز است،اما داده های ما ممکن است برای به حداقل رساندن خطر ابتلا به AMI در بازماندگان COVID-19 مفید باشد اما قابل استناد برای دریافت رژیم دارویی شامل ضد پلاکت ها و ضد لخته ها در بالین نیست.
۴.۱. محدودیت ها
مطالعه ما محدودیتهای متعددی در رابطه با ماهیت مشاهدهای مطالعات بررسیشده با تمام سوگیریهای موروثی آنها دارد. دست کم گرفتن احتمالی بروز AMI می تواند ناشی از عدم وجود یک پیگیری مشخص و اختصاصی باشد. در واقع، بخش بزرگتری از مقالات بررسی شده، وقوع AMI ها را از مجموعه داده های سوابق پزشکی بزرگتر با استفاده از کدهای نسبی ICD-10 شناسایی کردند و مشخص است که این رویکرد شناختی حساسیت کمی برای تشخیص AMI در جمعیت عمومی دارد. علاوه بر این، مطالعات کمی خطر ابتلا به AMI را در بیماران بهبود یافته از عفونت COVID-19 مورد تجزیه و تحلیل قرار داده اند که این مساله تعداد مشاهدات موجود در متاآنالیز را محدود می کنند. با این حال، تعداد بیماران ثبت نام شده، حداقل تا حدی، این محدودیت را کاهش می دهند. ما نمیتوانیم این نکته را رد کنیم که سوگیری در جمع آوری نمونه ممکن است منجر به دست کم گرفته شدن میزان وقوع تجمعی واقعی AMI شده باشد. به طور مشابه، هیچ داده ای در مورد نوع و تعداد واکسیناسیون علیه SARS-CoV-2 و همچنین بیماران مبتلا به AMI در مرحله حاد عفونت به طور سیستماتیک گزارش نشده است، که هر نوع تجزیه و تحلیل فرعی را غیرممکن می کند. به همین ترتیب، فقدان اطلاعات در مورد انواع مختلف COVID-19 نتایج ما را محدودتر کرده است. در نهایت، دادههای بررسیشده ممکن است تأثیر واقعی AMI پس از COVID-19 را بهویژه در مرحله اولیه همهگیری، هم به دلیل وجود موارد تشخیص داده نشده و هم به دلیل از دست دادن بیماران در طول دوره پیگیری، دست کم گرفته شده باشد. علیرغم این محدودیتها، تا جایی که ما میدانیم، این مطالعه اولین مرور سیستماتیک و متاآنالیز است که تخمین روشنی در مورد بروز و خطر ابتلا به AMI در بیماران بهبود یافته از COVID-19 ارائه میکند.
۵. نتیجه گیری ها
AMI یک عارضه نسبتاً نادر اما بالقوه پس از عفونت حاد با COVID-19 در دوره طولانی مدت است که ممکن است از استراتژی های پیشگیرانه تهاجمی و پیگیری مناسب بیماران COVID-19 بهره مند شود.