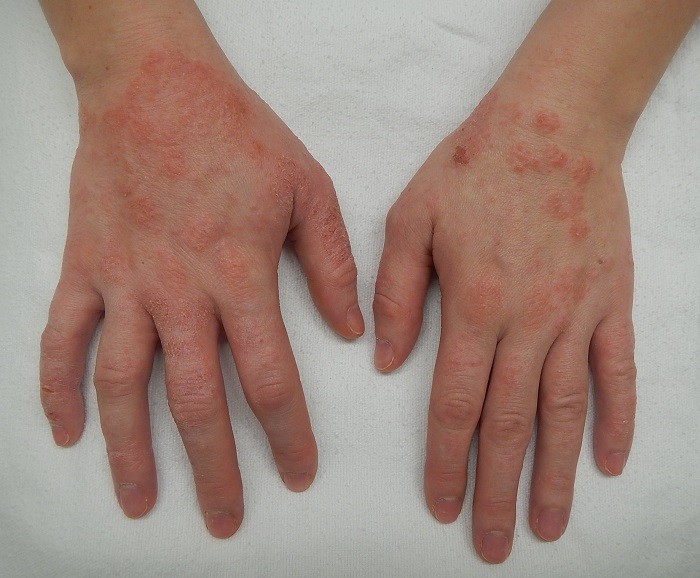
اساس ژنتیکی اتوپی
بیماری های آلرژیک وضعیت های ژنتیکی پیچیده ای هستند که به محرک های محیطی حساسندچندین گروه عمده از ژن ها با بیماری های آلرژیک همراهند: ژن هایی که بیان سیستمیک اتوپی را تنظیم می کنند (افزایش سنتز IgE ،ائوزینوفیلی، پاسخ های ماست سل) که به طور شایع در بیماری های آلرژیک مختلف بیان می شوند ، ژن هایی که عملکرد سد محافظتی را در ارگام های هدف مختلف کنترل می کنند ( پوست در درماتیت آتوپیک، ریه در آسم، دستگاه گوارش
در آلرژی غذایی)، و ژن های کدکننده recognition-Pattern از سیستم ایمنی ذاتی که عوامل بیماریزای میکروبی را جذب کرده و روی پاسخ ایمنی اکتسابی اثر می گذارند . وقتی پاسخ های آلرژیک شروع شد ، استعداد ژنتیکی در التهاب آلرژیک مزمن و پاسخ های انحرافی آسیب ترمیم در بازسازی بافتی و بیماری مداوم
شرکت می کنند.
بیماری های اتوپیک استعداد خانوادگی قوی دارند، با قابلیت توارث ۶۰ درصد که در مطالعات دوقلویی روی آسم و درماتیت آتوپیک دیده است . ناحیه ۳۵-5q23 شامل ژن های مختلفی است که سایتوکاین های Th2 را کد می کنند ( GM-CSF,IL-13,IL-9,IL-5 3-IL,4-IL ) و در پاتوژنز بیماری های آلرژک شرکت دارند . دربین اینها، ۴-IL ژن کاندیدی است که به خوبی مطالعه شده است. تغییر نوکلئوتیدی درموقعیت ۵۸۹ ناحیه پروموتوژن ۴-IL باتشکیل یک محل اتصال انحصاری برای فاکتور رونویسی AT-NF (فاکتور هسته ای سلول های T فعال شده ) ، افزایش رونویسی ژن ۴-IL، تمایل AT-NF برای اتصال بیشتر و افزایش تولید IgE به همراه است .به طور مشابه واریانت های کد کننده ناحیه ۱۳-IL با آسم و درماتیت اتوپیک همراه بوده اند.همراهی بین اتوپی و یک پلی مورفیسم کسب عملکرد روی کروموزوم۱۶ که زیر واحد a را در 4R-IL کد می کند، پیدا شده است. این یافته با نقش مهم ۴-IL و ۱۳-IL و گیرنده هایشان در ایمونوپاتوژنز بیماری های آلرژیک همراه است .
چندین جستجوی wide-genome نیز اتوپی رابه ناحیه کروموزوم 11q13 ارتباط داده اند . ژن کاندید پیشنهاد شده این ناحیه ،ژن زیر واحدB در B-FcERI است. ژن زیر واحدB فعالیت B-FCERI با آسم و درماتیت اتوپیک همراه بوده اند.
کروموزوم ۶ محتوی ژن های کد کننده مولکول های آنتی ژن لکوسیت انسانی (HLA) کلاس I و II است که اختصاصی بودن و قدرت پاسخ های ایمنی به آلرژن های اختصاصی را تنظیم می کند. پاسخ های IgE به آلژن های اختصاصی ،مانند آنتی ژن را گوید V a Amb و آلرژن مایت P1 Der با لوکوس خاص MHC کلاس II مرتبط بوده اند . a-TNF یک سایتوکاین کلیدی است که در ورود سلول های التهابی شرکت دارد ، نیز روی کروموزوم ۶ واقع شده است . پلی مورفیسم های a-TNF با آسم همراه بوده اند.
اختلال عملکرد سدی در پاتوژنز بیماری های آلرژیک نقش کلیدی دارد. مطالعات ارتباط ژنتیکی درماتیت اتوپیک اهمیت کروموزوم 1q21 که محتوی تجمعی از ژن های درگیر در تمایز اپیدرم است را نشان داده اند این امر در مطالعاتی که در بر گیرنده ژن های کد کننده فیلاگرین ، یک پروتئین ضروری برای تشکیل استراتوم کورنئوم است بهتر نشان داده شده که مکرراً نتیجه گرفته اند که موتاسیون های خنثی (null) ژن فیلاگرین همراهی قوی با شروع زود و شدید درماتیت اتوپیک دارند . نشان داده شده که جهش های ژن کد کننده مهار کننده سرین پروتئاز SPINK5 باعث بیماری Netherton می شود که یک اختلال تک ژنی همراه با اریترودرمی ، آلرژی غذایی و سطح سرمی باالی IgE است . یک پلی مورفیسم شایع در SPINK5( به خصوصG1u420Lys) خطر ایجاد درماتیت اتوپیک و آسم را افزایش می دهد . SPINK5 روی اپیدرم خارجی بیان می شود و تصور می شود که در خنثی سازی فعالیت پزوتئولیتیک استافیلوکوکوس اورئوس و آلرژن های شایعی مانند P1 Der که از این پروتئازها برای نفوذ به پوست و القا پاسخ های آلرژیک استفاده می کنند، مهم است . اختلال عملکرد سدی در سایر بیماری های آلرژیک ، مانند آسم و رینوسینوزیت دخالت دارد . ولی آحتماال سایر ژن های سدی ، مانند ژن های کد کننده اتصاالت شکاف ها (junction gap ) را دربر می گیرد . ژن های کاندید همراه با حساسیت به آسم توسط کلونینگ موقعیتی شناسایی شده اند: GPRA( گیرنده ممزوج شده با پروتئینG برای حساسیت به آسم روی کروموزوم 7P14) و ۳۳-ADAM ( یک دیس اینتگرین متالوپروتئاز۳۳ روی کروموزوم20P) ریا، وDPP10( دی پپتیدیل پپتیداز۱۰روی کروموزوم2q14). عملکرد این ژن ها در مسیرهای کالسیک اتوپی نمی گنجد و بنابراین دیدگاه های جدیدی در پاتوژنز آسم باز می کنند. GPRA یک گیرنده ممزوج با پروتئین G را کد می کند . با ایزوفرم هایی که روی سلول های اپی تلیال برونش و عضالت صاف اشخاص آسمی بیان می شوند، که نشانه نقش مهم این بافت ها در آسم است. ۳۳-ADAM درعضالت صاف برونش بیان شده با افزایش پاسخ دهی برونش مرتبط بوده است. DDP10 یک دی پپتیدیل پپتیداز را کد می کند که دو پپتید نهایی را از کموکاین های پیش التهابی خاص بر می دارد،تغییری که ممکن است التهاب آلرژیک را تعدیل کند.
گیرنده های تشخیص پاترن سیستم ایمنی ذاتی که روی سلول های اپی تلیال و دندریتیک ها بیان می شوند ، همراه با استعداد به بیماری بوده اند. این گیرنده ها اجزاء میکروبی خاصی را تشخیص می دهند.پلی مورفیسم های CD14 (اندوتوکسین را دربر می گیرد) گیرنده (like-2Toll(TLR2 (که استاف اورئوس را دربر می گیرد) و حوزه (domain) ایمونوگلوبولین سلولT و موسین که ویروس هپاتیتA را دربر می گیرد) با استعداد به آسم و یا درماتیت آتوپیک مرتبط بوده اند. اختلال تنظیم این سیستم ایمنی دفاع خط اول ممکن است منجر به پاسخ غیرطبیعی به آلرژین های محیطی شایع شود.