پس زمینه
بیماری کروناویروس ۲۰۱۹ (COVID-19) یک سندرم بالینی پیچیده است که توسط سندرم حاد تنفسی ویروس کرونا ۲ (SARS-CoV-2) ایجاد میشود. علیرغم بسیاری از مطالعات بزرگ که منجر به تایید اثر بخشی واکسن ها و ضد ویروس ها شده است، گسترش جهانی SARS-CoV-2 همچنان ادامه دارد. تا ۱۸ ژوئن ۲۰۲۲، بیش از ۵۳۵،۸۶۳،۹۵۰ مورد تایید شده در سراسر جهان، از جمله ۶،۳۱۴،۹۷۲ مرگ (براساس سازمان بهداشت جهانی) وجود داشته است.. به طور خاص، بیماریهای همراه سلامت و فعالیت بدنی اولیه ممکن است بیماران را مستعد افزایش خطر پیامدهای ناگوار پس از عفونت COVID-19 کند.
مطالعات قبلی نشان داده اند که دیابت شیرین (DM) با افزایش خطر ابتلا به کووید-۱۹ شدید، سندرم زجر تنفسی حاد (ARDS) و مرگ و میر در بیمارستان مرتبط است. جالبتر اینکه، یک متاآنالیز اخیر گزارش داده است که دیابت تازه تشخیص داده شده معمولاً در بیماران COVID-19 مشاهده میشود. جهان نگرانی هایی را در مورد رابطه دو طرفه بین این دو وضعیت بهداشتی مطرح کرده است.
با پیشرفت همهگیری کووید-۱۹، شواهد فزایندهای وجود دارد که نشان میدهد پس از مرحله حاد بیماری، افراد مبتلا به کووید-۱۹ میتوانند عواقب طولانی مدتی (به نام «کووید طولانی») ایجاد کنند که ممکن است شامل تظاهرات سیستم ریوی و خارج ریوی باشد، مانند دیابت . پیگیری کودکان مبتلا به COVID-19 نشان داده است که بروز دیابت نوع ۱ تازه تشخیص داده شده افزایش یافته است. یک متاآنالیز ثبت نشده در PROSPERO همچنین نشان داد که خطر ابتلا به دیابت در بزرگسالان مبتلا به کووید-۱۹ طولانی مدت وجود دارد، اما دارای اشکالاتی در طراحی مطالعه است که تفسیر و کاربرد یافتههای مطالعات فردی را محدود میکند. بنابراین، نیاز فوری به بررسیهای سیستماتیک و متاآنالیز مطالعات موجود، به ویژه با تمرکز بر مطالعات کنترلشده وجود دارد.
این مرور سیستماتیک و متاآنالیز برای تخمین شیوع یک تشخیص جدید دیابت پس از COVID-19 در مقایسه با انواع غیر مرتبط با کووید انجام شد.
مواد و روش ها
این مرور مطابق با متاآنالیز مطالعات مشاهدهای در اپیدمیولوژی (MOOSE) و دستورالعملهای گزارشدهی ترجیحی برای مرور سیستماتیک و متاآنالیز (PRISMA) و با توجه به روشهایی که در کتابچه راهنمای کاکرین برای بررسیهای سیستماتیک شرح داده شده است، انجام و گزارش شد. مداخلات (پرونده اضافی ۲: جدول S1 و جدول S2). پروتکل مطالعه در ۲۴ ژوئن ۲۰۲۲ در PROSPERO ثبت شد (شماره ثبت: CRD42022330723). از آنجایی که همه دادههای وارد شده از مطالعات منتشر شده قبلی بود، نیازی به تایید هیئت بررسی سازمانی نبود.
استراتژی جستجو و معیارهای واجد شرایط بودن
ما به طور سیستماتیک پایگاههای کتابشناختی الکترونیکی زیر را جستجو کردیم: PubMed، Embase، Web of Science، و سازمان ثبت مرکزی کارآزماییهای کنترلشده کاکرین. هیچ محدودیت زمانی یا زبانی برای نتایج جستجو اعمال نشد. به طور خلاصه، ترکیبی از عبارات جستجو شده شامل COVID-19 یا SARS-CoV-2، دیابت شیرین، دیابت یا DM بود. جستجو از ابتدا تا ۱۰ ژوئن ۲۰۲۲ انجام شد.
برای گنجاندن در این بررسی سیستماتیک، مطالعات کوهورت آیندهنگر یا گذشتهنگر باید تمام معیارهای زیر را برآورده میکرد: (۱) مواجهه با COVID-19 که بر اساس کدهای طبقهبندی بینالمللی بیماریها (ICD) تعریف شد. (۲) برای تعیین ارتباطات احتمالی، از جمعیت کنترل و مبتلایان بهعنوان معیار مقایسه استفاده شد. (۳) گزارش DM تازه تشخیص داده شده که به عنوان شروع جدید دیابت تعریف شده است (بدون سابقه قبلی دیابت با گلوکز پلاسما ناشتا [FPG] ≥ ۷.۰ mmol/L یا قند خون تصادفی [RBG]≥ ۱۱.1mmol/L یا HbA1c > 6.5٪. مطالعات زیر حذف شدند: گزارش های موردی یا سری موارد، بررسی ها، تفسیرها و نامه ها.
عواقب
پیامد اولیه، بروز DM تازه تشخیص داده شده پس از تشخیص عفونت SARS-CoV-2 و خطر نسبی ابتلا به DM در مقایسه با کنترلهای امروزی یا تاریخی در گروه غیر SARS-CoV-2 بود. ما آنالیزهای زیرگروهی را بر اساس سن، جنس، نوع دیابت، زمان شروع و اینکه آیا گروه کنترل دچارعفونت مجرای تنفسی فوقانی بود انجام دادیم. ما همچنین دو تجزیه و تحلیل زیرگروهی را انجام دادیم: بیماران مبتلا به کووید خفیف تا متوسط در مقابل بیماران مبتلا به کووید شدید، مورد بررسی در سه زمان مختلف پیگیری بعد از کووید-۱۹ (کمتر از ۳ ماه، ۳ تا ۶ ماه، و بیشتر از ۶ ماه) .
انتخاب مطالعه و استخراج داده ها
استخراج داده ها از مطالعات واجد شرایط با استفاده از یک Spreadsheet استاندارد شده انجام شد. دادههای استخراجشده شامل موارد مربوط به طراحی مطالعه و منابع داده، ویژگیهای شرکتکننده در مطالعه، تعریف مطالعه COVID-19، تعریف دیابت، متغیرهای کمکی، و تعداد سالهای پیگیری فرد (چه گزارششده یا قابل محاسبه) بود. داده ها توسط بازبین اول (TZ) استخراج و توسط بازبین دوم (QMM) دوبار بررسی شد. اختلاف نظر بین دو داور با بحث و گفتگو با داور سوم (YCL) حل شد.
کیفیت روش شناختی
خطر سوگیری برای مطالعات وارد شده با استفاده از مقیاس ارزیابی کیفیت نیوکاسل-اتاوا برای مطالعات کوهورت ارزیابی شد. ارزیابی انتقادی توسط سه بازبین (TZ، QMM، و YCL) انجام شد، اختلافات با گروه نویسندگان بزرگتر برای رسیدن به یک اجماع مورد بحث قرار گرفت.
تحلیل آماری
برای هر مطالعه وارد شده، بروز DM تازه تشخیص داده شده با استفاده از تعداد گزارش شده موارد دیابت تازه تشخیص داده شده و فرد-سال پیگیری محاسبه شد. ما ابتدا نسبت ها را با استفاده از روش آرکسین دوگانه فریمن-توکی تغییر دادیم و سپس یک متاآنالیز واریانس با اثرات تصادفی معکوس (DerSimonian و Laird) برای محاسبه برآوردهای تلفیقی انجام دادیم. میزان دیابت بین بیماران SARS-CoV-2 و افراد کنترل با استفاده از خطر نسبی (RR) با فاصله اطمینان ۹۵٪ (CIs) گزارش شد.
ناهمگونی بین مطالعات وارد شده با آمار کوکران Q و I2 ارزیابی شد. برای تفسیر کیفی ناهمگنی، مقادیر I2 حداقل ۵۰ درصد در نظر گرفته شد که نشان دهنده ناهمگنی قابل توجهی است، و مقادیر حداقل ۷۵ درصد نشان دهنده ناهمگنی قابل توجهی است. سطح معنی داری برای آماره Q 0.1 تعیین شد. برای پیامدهای گزارش شده در ۱۰ مطالعه یا بیشتر، سوگیری انتشار با ساختن نمودارهای زنگوله ای تقویت شده و آزمون Egger مورد بررسی قرار گرفت.
برای در نظر گرفتن اینکه چگونه عوامل مخدوش کننده کنترل نشده در هر مطالعه متاآنالیز شده باید برای نفی نتایج مشاهده شده باشد، یک تحلیل حساسیت را برای متاآنالیزهایی که مشابه ارزش E هستند، اعمال کردیم. ما یک ارزش E را محاسبه کردیم که نشاندهنده حداقل نقاط قوت ارتباط در مقیاس نسبت ریسک است که عوامل مخدوشکننده کنترلنشده باید به طور مشترک با COVID-19 و با DM در تمام مطالعات در هر متاآنالیز داشته باشند تا تخمین متا آنالیز تغییر کند و یا CL 95 آن به سمت صفر میل کند.
همه برآوردهای ریسک با ۹۵% CI مربوطه محاسبه شد. مقادیر p<0.05 از نظر آماری معنی دار در نظر گرفته شد. تمامی تحلیلهای آماری با نرمافزار R (نسخه ۴.۱.۲، وین، اتریش)، با استفاده از بستههای «metafor»، «EValue»، «confoundedmeta»، «metaviz» و «metaUtility» انجام شد.
نتایج
حاصل جستجو ۷۷۴۶ سند بود. پس از حذف موارد تکراری و بررسی عناوین و چکیده ها، ۷۵۴۳ مقاله حذف شدند. از ۲۰۳ مطالعه باقی مانده، ۱۹۶ مقاله تمام متن در دسترس بود. از ۱۹۶ مورد، ۱۸۷ مورد پس از بررسی نسخه های خطی کامل حذف شدند. پس از چند مرحله مرور، ۹ مطالعه واجد شرایط (با ۱۰ کوهورت) که شامل متاآنالیز و هشت مطالعه همگروهی تطبیق امتیاز تمایل (PSM) بودند شامل شد (شکل ۱).
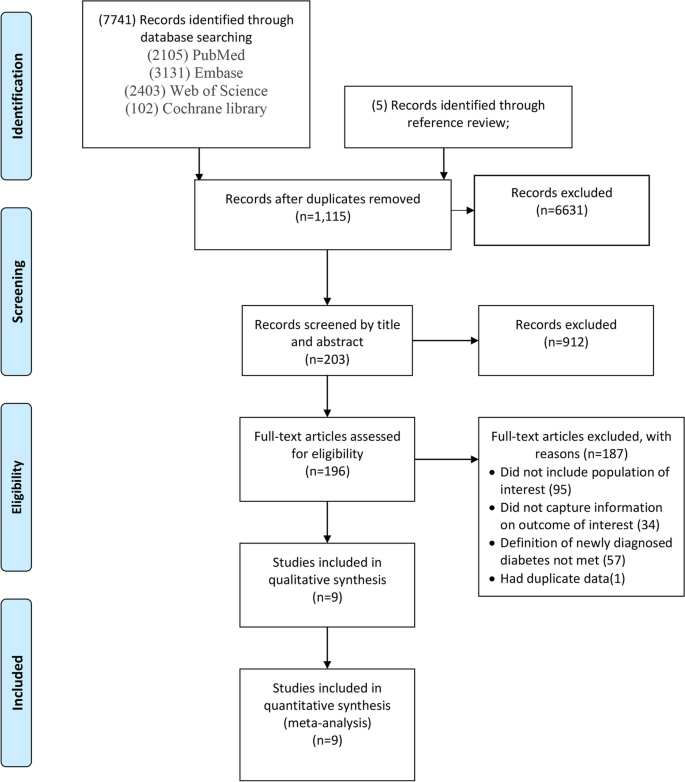
جدول ۱ و جدول S2 ویژگی های مطالعات وارد شده را نشان می دهد: ۶ مطالعه در ایالات متحده آمریکا، دو مورد در انگلستان و یک مطالعه در آلمان انجام شده است. از میان نه مطالعه، هفت مطالعه فقط بزرگسالان، یک مطالعه شامل جمعیت کامل (بدون محدودیت)، و یک مطالعه فقط شامل نوجوانان بود. به طور کلی، ۴,۰۰۲,۴۷۵ نفر مبتلا به کووید-۱۹ و ۳۴,۷۱۷,۴۲۲ نفر در گروههای کنترل مربوطه بودند.
خطر سوگیری در مطالعات کوهورت شامل با استفاده از مقیاس نیوکاسل-اتاوا ارزیابی شد و در جدول S3 ارائه شده است. نمره کلی ۸۸ از ۹۰ (۹۷.۸٪) بود که خطر نسبتاً پایینی برای سوگیری در نظر گرفته می شود.
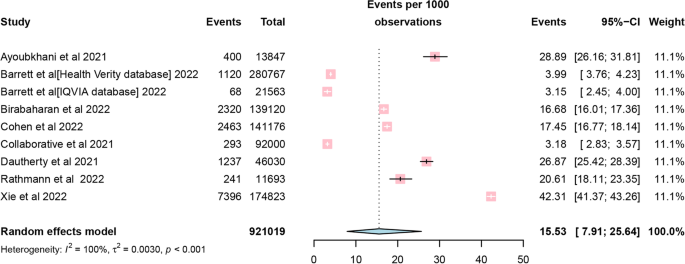
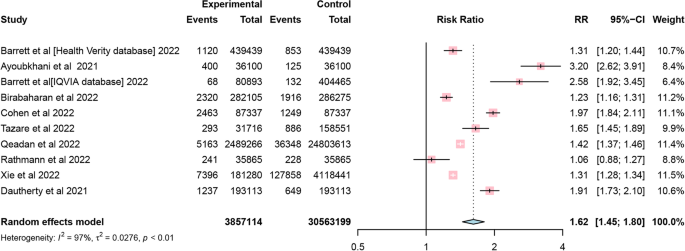
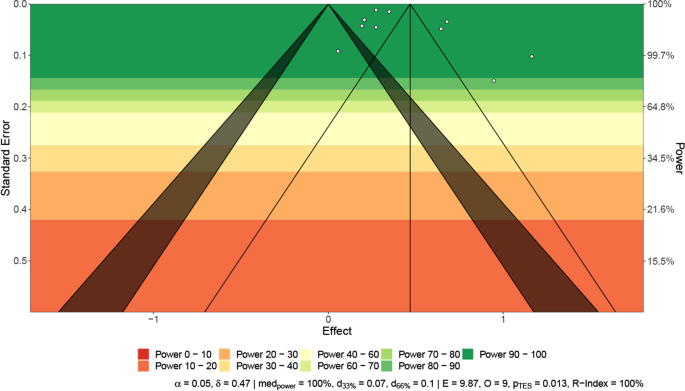
از ۹ مطالعه وارد شده، اگرچه یک مطالعه فاقد زمان پیگیری خاص بود،اما ، با استفاده از یک متاآنالیز اثرات تصادفی بروز کلی دیابت ۱۵.۵۳ مورد در هر ۱۰۰۰ نفر-سال پیگیری ، محاسبه شد ([۹۵% فاصله اطمینان (CI 7.91-25.64]؛ شکل ۲) . خطر نسبی دیابت پس از COVID-19 در مقایسه با بیمارانی که به COVID-19 آلوده نشده بودند، ۱.۶۲ بود ([۹۵% فاصله اطمینان (CI): 1.45-1.80]؛ شکل ۳. نمودارهای زنگوله ای تقویت شده و آزمون Egger (0.104 = p) سوگیری انتشار را مطرح نکردند (شکل ۴). پس از این بررسی های نموداری متوجه شدیم که همه مطالعات دارای آزمونهای آماری قوی هستند.
تجزیه و تحلیل زیر گروهی با بررسی نوع دیابت تازه شروع شده انجام شد. خطر ابتلا به دیابت نوع ۱ (وابسته به انسولین) با متاآنالیز RR=1.48 بود ([۹۵% فاصله اطمینان (CI): 1.26-1.75]؛ دیابت نوع ۲ (غیر وابسته به انسولین) دارای RR 1.70 بود ([۹۵% فاصله اطمینان (CI): 1.32-2.19]؛ و افراد مبتلا به نوع نامشخص دیابت دارای RR 1.50 ([95% فاصله اطمینان (CI 0.87-2.58] در مقایسه با جمعیت غیر آلوده بودند.
تجزیه و تحلیل زیرگروهی دیگری با توجه به اینکه آیا گروه کنترل مبتلا به عفونت دستگاه تنفسی فوقانی بودند یا نه، انجام شد. خطر نسبی ابتلا به دیابت ۱.۱۷ برابر ([۹۵% فاصله اطمینان (CI 1.02-1.34]؛ پس از COVID-19 در مقایسه با بیماران مبتلا به عفونتهای دستگاه تنفسی فوقانی افزایش یافت. خطر نسبی ابتلا به دیابت ۱.۸۲ برابر ([۹۵% فاصله اطمینان (CI): 1.47-2.24] ) پس از COVID-19 در مقایسه با جمعیت عمومی افزایش یافت.
آنالیز زیرگروهی مجدداً با توجه به سن شروع انجام شد. نرخ بروز سالانه به ازای هر ۱۰۰۰ نفر-سال پیگیری ۳.۶۵ (۹۵% فاصله اطمینان (CI)، ۲.۹۱-۴.۸۳؛ )در افراد کمتر از ۱۸ سال بود ۱۵.۵۳ ([۹۵% فاصله اطمینان (CI): 7.91-25.64]؛ ) در افراد بالای ۱۸ سال و ۱۷.۴۵ ([۹۵% فاصله اطمینان (CI): 16.77-18.14]؛ در افراد بالای ۶۵. در تمام سنین، بین عفونت کووید-۱۹ و خطر ابتلا به دیابت همبستگی مثبت و معنادار آماری وجود داشت. همبستگی مثبت بین عفونت COVID-19 و خطر ابتلا به دیابت از نظر آماری در تمام سنین، <18 سال معنیدار بود: RR=1.72 ([95% فاصله اطمینان (CI): 1.19-2.49]؛ ). ≥۱۸ سال: RR=1.63 ([95% فاصله اطمینان (CI): 1.26-2.11]؛ ). >65 سال: RR=1.68 ([95% فاصله اطمینان (CI): 1.22-2.30]؛ ).
در نهایت تجزیه و تحلیل زیر گروهی بر اساس جنسیت انجام شد. میزان بروز ۳.۱۴ ([۹۵% فاصله اطمینان (CI): 0.75-7.15]؛ ) به ازای هر ۱۰۰۰ نفر-سال پیگیری در جمعیت مرد و ۳.۰۰ ([۹۵% فاصله اطمینان (CI): 0.80-6.59]؛ =) به ازای هر ۱۰۰۰ نفر-سال پیگیری در جمعیت زن بود. خطر نسبی ابتلا به دیابت در مردان ۲.۰۸ برابر ([۹۵% فاصله اطمینان (CI): 1.27-3.40]؛) و ۲.۱۵ برابر در زنان ([۹۵% فاصله اطمینان (CI): 1.26-3.68] ) بعد از COVID-19 در مقایسه با جمعیت بدون عفونت COVID-19 بود.
میانگین زمان پیگیری شرکت کنندگان بین ۶۴ تا ۳۵۲ روز بود. بروز تجمعی دیابت گزارش شده در دوره های زمانی مختلف پیگیری ۲.۱۹٪ (۹۵٪ فاصله اطمینان (CI): 1.36-3.21) در کمتر از ۳ ماه، ۴.۴۶٪ (۹۵٪ فاصله اطمینان (CI): 0.40-12.53) بود. در ۳ تا ۶ ماه، ۰.۹۱٪ (۹۵٪ فاصله اطمینان (CI): 0.05-2.82) در بیش از ۶ ماه بوده است. علاوه بر این، خطر ابتلا به دیابت تازه شروع به طور قابل توجهی در محدوده پیگیری گزارش شده شناسایی شد: RR 1.95 در کمتر از ۳ ماه (۹۵% فاصله اطمینان (CI): 1.85-2.06)، RR 1.24 در ۳ تا ۶ ماه (۹۵% فاصله اطمینان (CI): 1.12-1.37) و RR 1.38 در بیش از ۶ ماه (۵% فاصله اطمینان (CI): 1.23-1.55) گزارش شد.
در میان مطالعات وارد شده، بیماران در شش مطالعه کوهورت از COVID-19 خفیف تا متوسط رنج می بردند. بیماران در سه مطالعه شامل بیماران خفیف، متوسط و شدید بودند. تنها یک مطالعه سطوح حدت بیماران COVID-19 را تجزیه نکرد. تجزیه و تحلیل زیرگروهی نشان داد که در مقایسه با بیماران غیر COVID-19، بروز دیابت در گروه خفیف تا متوسط ۲.۹%بود. ([۹۵٪ فاصله اطمینان (CI 0.58-7.07]؛ و خطر ۱.۴۸ برابر بود ([۹۵% فاصله اطمینان (CI): 1.25-1.75]؛). بروز دیابت در بیماران شدید ۱۱.۶۵% بود ([۹۵% فاصله اطمینان (CI): 2.59-25.96]؛)، و خطر ۱.۶۷ برابر بود ([۹۵% فاصله اطمینان (CI): 1.25-2.23]؛).
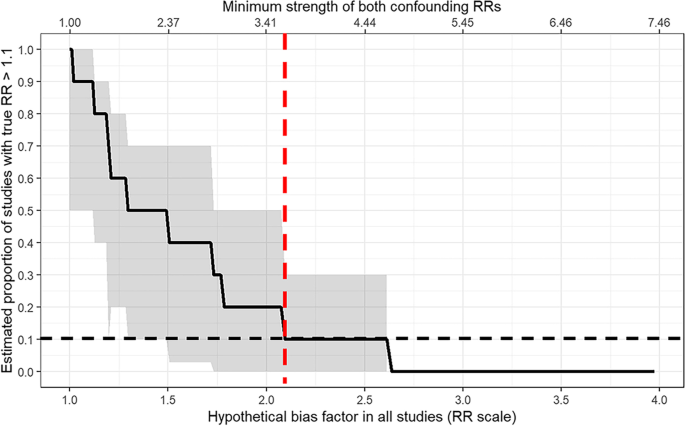
آنالیز حساسیت برای آشفتگی های آماری اندازه گیری نشده نشان داد که برای کاهش درصد RR بالای ۱.۱ از ۱۰۰ به ۱۰٪، ما ضریب سوگیری حداقل ۲.۰۸ ([۹۵% فاصله اطمینان (CI 1.55-2.84]؛ شکل ۵) را در هر یک مورد باید در نظر بگیریم. این بدان معنی است که آشفتگی های اندازه گیری نشده باید تخمین نقطه هر مطالعه را ۲.۰۸ برابر در مقیاس RR از نقطه صفر دور کند. با استفاده از معیار E-value، این عامل سوگیری معادل عوامل مخدوشکننده اندازهگیری نشده در هر مطالعه است که هم کووید-۱۹ و هم دیابت را با نسبتهای خطر حداقل ۳.۵۸ در هر یک تحت تأثیر قرار میدهد ([۹۵% فاصله اطمینان (CI): 2.43-5.12]؛).
بحث
این بررسی سیستماتیک و متاآنالیز برآوردهای کمی جامعی از بروز دیابت در ۱۰ جمعیت پس از COVID-19 ارائه کرد. طبق دانش ما، این بزرگترین و گسترده ترین تحلیل از این نوع تا به امروز است. با نزدیک به ۴۰ میلیون شرکتکننده و نزدیک به ۲۰۰۰۰۰ مورد دیابت گزارش شده، ما بروز دیابت پس از COVID-19 را در هر ۱۰۰۰ نفر در سال ۱۵.۵۳ و خطر نسبی ۱.۶۲ در مقایسه با افراد غیر آلوده به COVID-19 را یافتیم. تجزیه و تحلیلهای زیرگروهی نشان داد که خطر ابتلا به دیابت بدون در نظر گرفتن سن، جنسیت، نوع دیابت، زمان پیگیری یا سطح شدت COVID-19 نیز افزایش مییابد، اگرچه دیابت تمایز نیافته خطر نسبی قابلتوجهی ندارد. این نتایج حتی پس از در نظر گرفتن احتمال اشتباه اندازهگیری نشده باقی ماندند.
نتایج مشابهی در بیماران آلوده به ویروس های دیگر گزارش شده است که با افزایش بروز دیابت در مقایسه با افراد غیر آلوده مرتبط است. تجزیه و تحلیل زیر گروه ما نشان داد که خطر ابتلا به دیابت پس از COVID-19 در مقایسه با بیماران مبتلا به سایر عفونتهای دستگاه تنفسی فوقانی ۱.۲ برابر و خطر ابتلا به دیابت پس از COVID-19 در مقایسه با جمعیت عمومی ۱.۸۲ برابر افزایش یافته است. این نیاز به توجه پزشکان به متابولیسم گلوکز بیماران در مرحله پس از حاد COVID-19 را تقویت می کند.
همچنین شواهد جدیدی در مورد تأثیر ویروس SARS-CoV-2 بر عملکرد سلول های بتا پانکراس وجود دارد. پیشنهاد شده است که SARS-CoV-2 ممکن است با تأثیر بر mRNA آنزیم مبدل آنژیوتانسین ۲ (ACE2) در غدد درون ریز و برون ریز پانکراس، پانکراس را تحت تأثیر قرار دهد. وجود آنتی ژن SARS-CoV-2 اخیراً در پانکراس پس از مرگ بیمارانی که بر اثر کووید-۱۹ فوت کرده اند گزارش شده است. علاوه بر این، SARS-CoV-2 میتواند یک طوفان سیتوکین ایجاد کند، یک پاسخ ایمنی اغراقآمیز که طیف وسیعی از سیتوکینها را تولید میکند، در نتیجه یک محیط پیش التهابی سیستمیک ایجاد میکند، که ممکن است در تقویت مقاومت به انسولین و تحریک بیش از حد سلولهای بتا نقش داشته باشد که در نهایت منجر به تغییر عملکرد سلولی و مرگ سلول های β می شود. بر اساس تجزیه و تحلیل زیر گروه ما، در مقایسه با بیمارانی که به کووید-۱۹ آلوده نشده بودند، ۱.۴۸ برابر افزایش خطر ابتلا به دیابت نوع ۱ و ۱.۷ برابر افزایش خطر ابتلا به دیابت نوع ۲ وجود داشت.
در تجزیه و تحلیل ما، میزان بروز به ازای هر ۱۰۰۰ نفر-سال پیگیری ۳.۶۵ (۹۵٪ فاصله اطمینان، ۲.۹۱ تا ۴.۸۳)، RR=1.72 (95٪ فاصله اطمینان، ۱.۱ تا ۲.۵۰) در جمعیت کمتر از ۱۸ سال بود که با نتایج مشابه در بزرگسالان و در افراد بالای ۶۵ سال همراه بود. علاوه بر این، خطر نسبی عوارض در بین جنسیت ها مشابه بود. این یافتهها بر اهمیت پیشگیری از COVID-19 در همه گروههای سنی و جنسیتی، تاکید میکند.
اگرچه همه مطالعاتی که ما عوامل مخدوش کننده را با تنظیم خطر عوامل مرتبط (تطابق نمره تمایل) وارد کردیم، اما نگرانی در مورد سوگیری احتمالی ناشی از عوامل مخدوش کننده کنترل نشده (مانند بیماری های همراه، محیط اجتماعی-اقتصادی، شاخص توده بدنی [BMI] و غیره .) باقی می ماند. مطالعه ما اولین متاآنالیز است که E-Value را به عنوان پارامتری از عوامل مخدوشکننده اندازهگیری نشده در بررسی ارتباط بین مرحله پس از حاد COVID-19 و خطر دیابت در نظر میگیرد، که نشاندهنده یک سهم روششناختی جدید در مطالعه COVID-19 و دیابت است. E-value، تحلیل حساسیت عوامل مخدوشکننده اندازهگیری نشده، روشی نسبتاً جدید برای اندازهگیری ارتباط بین قرار گرفتن در معرض و استحکام نتیجه و ارزیابی شواهد علی است. نتایج ما نشان میدهد که یک عامل مخدوشکننده مشاهده نشده باید با نسبت ریسک ۲.۰۸ برای قرار گرفتن در معرض و نتیجه همراه باشد تا میانگین RR 1.62 را به طور کامل توضیح دهد. علاوه بر این، نسبت ریسک ۳.۵۸ برای عامل مخدوش کننده مورد نیاز است تا برآورد ریسک را از نظر آماری غیر قابل توجه نشان دهد. تطبیق گرایش در همه مطالعاتی که ما وارد کردیم انجام شد، و بیشتر مطالعات حداقل برای برخی از عوامل مخدوش کننده مهم بالینی، مانند سن بیمار، جنسیت، BMI، نژاد و بیماری های همراه تنظیم شدند. بنابراین، ما معتقدیم که وجود مخدوش کننده های باقیمانده، فراتر از این مخدوش کننده های اندازه گیری شده که برای توضیح نتایج فوق کافی هستند، غیرمحتمل است.
محدودیت ها
چندین محدودیت مطالعاتی بالقوه باید در نظر گرفته شود. اول، همه مطالعات وارد شده از یک طرح گذشته نگر استفاده کردند و همه مطالعات از وسعت و عمق پایگاههای اطلاعاتی مراقبتهای بهداشتی الکترونیکی بزرگ برای ساخت گروهها و تعریف ویژگیهای سلامت بر اساس تعاریف معتبر استفاده کردند. این ویژگی هایی که نمی توانند سوگیری طبقه بندی نادرست را به ویژه برای انواع دیابت حذف کنند. ثانیاً، برخی از مطالعات از کنترلهای معاصر استفاده میکردند، و این احتمال را که برخی از افراد ممکن است به SARS-CoV-2 آلوده شده باشند و مورد آزمایش قرار نگرفته باشند را رد نکردند، که اگر این افراد به تعداد زیاد در گروه کنترل معاصر وجود داشته باشند میتوانند نتایج را به سمت فرضیه صفر سوق دهد .سوما از آنجایی که مطالعات وارد شده در کشورهای مختلف و در مناطق مختلف در یک کشور انجام شده است، تفاوت در سیاست های مراقبت ملی و منطقه ای مورد انتظار است، که این متاآنالیز نمی تواند برای آنها تطبیق یا تعدیل شود. چهارم، طرح های مطالعه ناهمگن بودند (مطالعات کوهورت آینده نگر و همگروهی گذشته نگر). از آنجایی که تعداد مطالعات کوهورت آیندهنگر موجود در مورد این موضوع کم است، برای تأیید نتایج ما به مطالعات با کیفیت بیشتری نیاز داریم.

