مقدمه
کووید طولانی (LC) یک بیماری ناتوان کننده است که می تواند در هر فردی پس از عفونت SARS-CoV-2، مستقل از شدت بیماری COVID-19 ایجاد شود. LC به عنوان تجربه علائم در عرض سه ماه پس از عفونت اولیه تعریف می شود که حداقل دو ماه طول می کشد. علائم می تواند شامل خستگی، اختلال عملکرد شناختی، ضعف پس از تمرین (PEM)، سردرد، بی خوابی و دردهای عضلانی باشد. پاتوفیزیولوژی LC شامل اختلال در تنظیم ایمنی و خودایمنی، تداوم/فعال شدن مجدد عامل پاتوژن، ناهنجاری های عصبی و التهاب عصبی، آسیب بافت و اندام، هیپوپرفیوژن و اختلال عملکرد اتونومیک، میکرولخته های آمیلوئید فیبرین و اختلال در تنظیم میکروبیوم است. شواهد نشان می دهد که LC دو برابر بیشتر از مردان بر زنان تأثیر می گذارد و ممکن است به طور نامتناسبی بر افراد تراجنسیتی تأثیر بگذارد. زنان پیش از یائسگی در معرض خطر بالاتری برای LC هستند، که نشان می دهد هورمون های جنسی ممکن است نقش کلیدی در ایجاد LC داشته باشند. سلامت باروری (RH) هدف رایجی برای LC است، اما هنوز به طور قابل توجهی مورد مطالعه قرار نگرفته است. بررسی پیش رو شواهدی از علائم RH زنان را در بیماران LC بررسی میکند. با توجه به تحقیقات محدود، ما همچنین اثرات بیماریهای مرتبط از جمله آنسفالومیلیت میالژیک/سندرم خستگی مزمن (ME/CFS)، سندرم تاکی کاردی ارتواستاتیک وضعیتی (POTS)، اختلالات بافت همبند مانند اهلرز-دانلوس (EDS) و اندومتریوز را نیز بررسی میکنیم. همانند LC، این بیماری ها نیز عمدتاً زنان را تحت تأثیر قرار می دهند و ممکن است بررسی آنها به روشن شدن علت اختلال در سلامت باروری ناشی از LC کمک کنند. این بررسی اهمیت مطالعه RH در LC را نیز برجسته می کند، به خصوص که شرایط RH به طور کلی طی گذشت زمان کمتر مورد تحقیق قرار گرفته است.
۲. سلامت باروری زنان در کووید طولانی
مطالعات کمی تأثیر LC بر RH زنان را بررسی کرده اند، و تحقیقات در حال انجام نشان می دهد که LC می تواند بر چرخه قاعدگی، سلامت تخمدان ها و باروری تأثیر بگذارد.
۲.۱. کووید طولانی و چرخه قاعدگی
تحقیقات نشان داده است که زنانی که در سن پیش از یائسگی به سر میبرند و مبتلا به LC هستند ، ممکن است معمولاً تظاهراتی از بدتر شدن علائم LC در طی قبل از قاعدگی و یا قاعدگی را تجربه کنند. در یک مطالعه مقطعی (۱۷۹۲=n)، بیش از یک سوم از بیماران LC تشدید علائم قاعدگی را در هفته قبل یا در طول قاعدگی گزارش کردند. در مطالعه مقطعی دیگری (۴۶۰ نفر)، ۶۲ درصد از بیماران LC بدتر شدن علائم را در روزهای قبل از قاعدگی تجربه کردند. بیماران LC گزارش می دهند که بی نظمی در چرخه قاعدگی، از جمله تغییر در طول چرخه، مدت، و شدت قاعدگی را تجربه می کنند. در یک نظرسنجی انجام شده در بین بیمارانی از چند کشور مختلف ، از ۱۷۹۲ بیمار مبتلا به LC با سیکل قاعدگی فعال، ۳۳.۸٪ مشکلاتی را در قاعدگی گزارش کردند که شامل چرخه های غیرعادی نامنظم (۲۶٪) و پریودهای سنگین (۱۹.۷٪) بود. علاوه بر این، ۴.۵ درصد از ۱۱۲۳ زن ۴۹ ساله یا بالاتر، خونریزی پس از یائسگی را گزارش کردند. نظرسنجی دیگری نشان داد که بیماران LC (n = 748) نرخ بالاتری از تغییرات چرخه قاعدگی (OR 1.34، ۹۵% فاصله اطمینان (CI): 1.15-1.57) را در مقایسه با جمعیت عمومی گزارش میکنند، هم با سابقه مثبت کووید (n = 2299) و هم بدون سابقه مثبت (n = 15156) (OR 0.99، ۹۵% فاصله اطمینان (CI): 0.91-1.09). یک مطالعه کوهورت آیندهنگر طولی نشان داد که ۱۶ درصد از زنان تغییرات چرخه قاعدگی را ۲۸ تا ۲۲۲ روز پس از عفونت SARS-CoV-2 تجربه کردند . اینها شامل قاعدگی نامنظم و تشدید علائم PMS است. یک مطالعه مورد-شاهدی گذشته نگر با مقایسه اثرات COVID-19 (n = 1066) و واکسیناسیون (n = 4989) بر سلامت قاعدگی نشان داد که سابقه COVID-19 ( اما نه واکسیناسیون) با افزایش ریسک تغییرات در مدت چرخه قاعدگی، خونریزی بین قاعدگی ها، افزایش خونریزی طی قاعدگی و توقف قاعدگی همراه است. از محدودیتهای این مطالعات میتوان به فقدان گروههای کنترل و عدم غربالگری شرکتکنندگان از نظر بیماریهای مرتبط اشاره کرد که این عوامل ممکن است بر چرخههای قاعدگی تأثیر بگذارد، مانند واکسیناسیون.
۲.۲. کووید طولانی، باروری و سلامت تخمدان
گزارشهای موردی نشان میدهد که عفونت کووید-۱۹ ممکن است با کاهش سلامت تخمدان ها در طولانیمدت، از جمله نارسایی زودرس تخمدان (POI) قبل از ۴۰ سالگی همراه باشد. بر اساس سونوگرافی ترانس واژینال و بررسی هورمون محرک فولیکول (FSH) ،اختلال POI در یک بیمار ۳۴ ساله گزارش شد که از ۱۲ ماه قبل همزمان با عفونت COVID19، سیکل های قاعدگی نامنظم و خونریزی غیرطبیعی کم حجم را تجربه کرده بود. هفت ماه پس از COVID-19، یک بیمار LC ۳۴ساله دیگر به دلیل افزایش سطح گنادوتروپین و چرخه های قاعدگی نامنظم همراه با الیگومنوره، مبتلا به POI تشخیص داده شد. چرخه قاعدگی بیمار دو ماه قبل از ابتلا به کووید-۱۹ ، منظم بوده و سطح هورمونها نیز نرمال بود. هشت ماه پس از COVID-19، یک بیمار ۲۷ ساله که از زمان عفونت با کووید دچار آمنوره شده بود، بر اساس سطوح بالای هورمون های گنادوتروپین (FSH و LH) و سطوح استرادیول در دوران یائسگی، مبتلا به POI تشخیص داده شد. بیماران در این گزارشهای موردی برای بیماریهای مرتبط با LC (مانند ME/CFS یا POTS) غربالگری نشدند، که درک پاتوفیزیولوژی POI در LC را مختل میکرد. با توجه به اینکه فقط گزارشهای موردی وجود دارد، هیچ تخمینی از میزان بروز POI پس از COVID-19 یا ارتباط آن با بیماریهای مرتبط و اینکه آیا در بین افراد مبتلا به LC شایعتر است یا خیر وجود ندارد.نوع ترکیب مایع فولیکولی ممکن است ماهها پس از عفونت COVID-19 تغییر کند که میتواند بر کیفیت تخمک و باروری تأثیر بگذارد. سطوح سیتوکین IL-1 و فاکتورهای رشد اندوتلیال عروقی (VEGF) که پپتیدهای کلیدی در رگزایی و نفوذپذیری عروق و در نتیجه رشد تخمک تلقی میشوند، در مایع فولیکولی افرادی که تحت درمان کمک باروری در بازه زمانی ۲ تا ۹ ماه بعد از عفونت با کووید قرار داشتند (به طور متوسط ۴.۵ ماه) ( n = 46) پس از COVID-19 در مقایسه با گروه کنترلی که SARS-CoV-2 منفی بودند یا هرگز علائم COVID-19 نداشتند (n = 34) کمتر بود. یائسگی زودرس، همراه با خطرات درازمدت موثر بر سلامتی از جمله افزایش عوارض و مرگ و میر، در ۳ درصد از یک نمونه از ۹۳۸ زن مبتلا به LC در سن ۴۰ سالگی گزارش شد که به مدت ۷ ماه پس از کووید-۱۹ علائم پایدار داشتند. این یافته بالاتر از تخمینهای پیش از همهگیری در مورد یائسگی زودرس در میان زنان در ۴۰ سالگی است.
۲.۳. کووید طولانی و بارداری تعداد کمی
یک بررسی مقطعی در اکوادور نشان داد که زنان باردار (n = 16) و غیر باردار (n = 231) با LC علائم مشابهی از LC را تجربه کردند که با سه علامت شایع گزارش شده برای هر دو گروه بود :خستگی، ریزش مو و اختلال در تمرکز. یک مطالعه کوهورت آیندهنگر در ایالات متحده روی افراد باردار نشان داد که ۲۵٪ بیماران ، تظاهرات LC را در حدود هشت هفته یا بیشتر پس از مثبت شدن آزمایش SARS-CoV-2 داشتند. با این حال، مطالعات هنوز چگونگی تأثیر LC بر بارداری را بررسی نکرده اند. یک مطالعه کوهورت آیندهنگر کوچک اما مهم در برزیل ۸۸ نفر از زنان باردار را پس از مثبت شدن آزمایش کووید-۱۹ (۸۴ نفر) دنبال کرد و نشان داد که ۷۵.۹٪ به LC مبتلا شدهاند. این مطالعه همچنین نشان داد که بیمارانی که گلوکوکورتیکوئیدها برای درمان کووید-۱۹ در دوران بارداری دریافت میکردند، در معرض خطر بیشتری (RR 6.92، ۹۵% فاصله اطمینان (CI): 1.70-28.07) برای خستگی مداوم بودند که یک علامت کلیدی و ناتوان کننده LC است.
۳. سلامت باروری زنان در بیماری های همراه یا مرتبط با کووید طولانی: مروری کوتاه بر آنسفالومیلیت میالژیک/سندرم خستگی مزمن (ME/CFS)، سندرم تاکی کاردی ارتواستاتیک وضعیتی (POTS)، سندرم اهلرز-دانلوس (EDS) و اندومتریوز
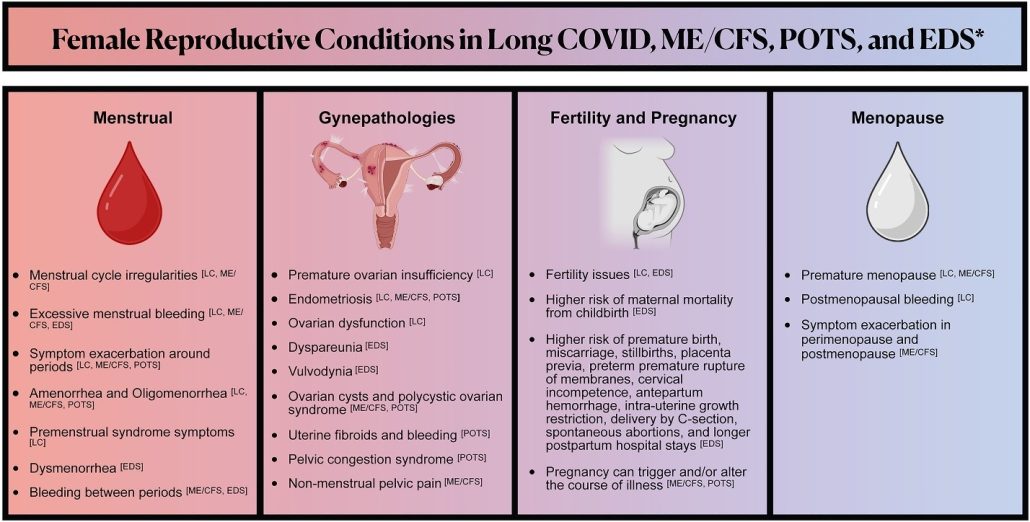
با توجه به حداقل تحقیقات در مورد شرایط RH در LC، ما از تحقیقات محدود و اغلب مقطعی در مورد RH در ME/CFS و POTS استفاده می کنیم – بیماری هایی که اغلب توسط عفونت ایجاد می شوند و بسیاری از افراد مبتلا به LC به آن مبتلا می شوند. علاوه بر این، ما تحقیقاتی را در مورد اختلالات بافت همبند، یعنی EDS، و اندومتریوز، بیماریهایی با پیامدهای RH قابل توجهی که با ME/CFS و POTS همراه هستند و ممکن است با LC مرتبط باشند، بررسی میکنیم. شکل ۱ را برای خلاصه ای از شرایط باروری زنان که در Long COVID، ME/CFS، POTS و EDS بررسی می کنیم، را میتوانید ببینید.
۳.۱. انسفالومیلیت میالژیک/سندرم خستگی مزمن
(ME/CFS) یک بیماری عصبی چند سیستمی که با علائم زیر مشخص میشود: علائم عصبی، عروقی ، شناختی، درد، خستگی شدید که با خواب تسکین نمی یابد و تشدید علائم پس از فعالیت فیزیکی (PEM). عفونت شایع ترین عامل شروع ME/CFS است که تا ۷۵ درصد موارد را تشکیل می دهد. جنسیت زن یک عامل خطر قابل توجه و ثابت برای ME/CFS است و جنسیت و رویدادهای غدد درون ریز بر روند بیماری تأثیر می گذارد. بسیاری از زنان مبتلا به ME/CFS گزارش می دهند که چرخه های قاعدگی، بارداری و یائسگی علائم را تشدید می کنند. در مقایسه با افراد سالم، زنان مبتلا به ME/CFS به طور نامتناسبی سیکل های قاعدگی نامنظم، آمنوره، خونریزی بیش از حد قاعدگی، خونریزی بین قاعدگی، درد لگنی غیرقاعدگی، آندومتریوز، PCOS، کیست های تخمدان ، قرار گرفتن تحت جراحی زنان (به ویژه هیسترکتومی هیسترکتومی) و سابقه هیسترکتومی را گزارش کرده اند. نیم تا دو سوم (۵۳٪-۶۷٪، n = 120 و n = 42) از بیماران زن ME / CFS افزایش علائم قبل از قاعدگی را گزارش کردند. یک مطالعه کنترل شده طولی (۱۵۷ نفر) نشان داد که یائسگی زودرس یک عامل خطر برای ME/CFS است. میانگین سن یائسگی در ME/CFS (37.6 سال) زودتر از افراد سالم (۴۸.۶ سال) بود که احتمالاً بخشی از آن به دلیل جراحی زنان است. در یک مطالعه پیمایشی مقطعی، یائسگی علائم را در ۳۸٪ (۱۵۰ نفر) از زنان یائسه و یائسه مبتلا به ME/CFS تشدید کرد. بارداری به عنوان یک محرک برای ME/CFS در ۳ تا ۱۰ درصد موارد گزارش شده است. یک مطالعه (۷۷ نفر) با سن، جنس و تحصیلات همسان کنترل نشان داد که زنانی که در سال گذشته باردار بوده اند بیش از ۳۱ برابر بیشتر در معرض ابتلا به ME/CFS هستند. شواهد برای علائم در میان بیماران ME/CFS که باردار میشوند متفاوت است.
۳.۲. سندرم تاکی کاردی ارتواستاتیک وضعیتی (POTS) و سلامت باروری
POTS نوعی دیساآتونومی است که شامل تاکی کاردی ارتواستاتیک بدون هیپوتانسیون ارتواستاتیک است. علائم شایع شامل سبکی سر، تاکی کاردی، پیش سنکوپ و سردرد است. در بین بیماران LC، ۲۸٪ و ۳۰٪ (n = 42,n=70) در دو مطالعه تست ناب ناسا و تست ایستاده فعال POTS داشتند. شیوع POTS قبل از همه گیری بین ۰.۲٪ تا ۱٪ تخمین زده می شود. قاعدگی می تواند به طور قابل توجهی بر علائم POTS تأثیر بگذارد. مشخص شده است که هورمونهای چرخه قاعدگی بر همودینامیک (برون ده قلبی، حجم سکته مغزی و مقاومت کلی محیطی) بیماران POTS تأثیر میگذارند، اما در افراد سالم نه که احتمالاً با تعدیل سیستم رنین-آنژیوتانسینالدوسترون این مساله رخ میدهد. افزایش استروژن و پروژسترون در فازهای میانی لوتئال ممکن است احتباس حجم خون را افزایش دهد و با افزایش سطح هورمون های کلیوی-آدرنال همراه است. یک مطالعه آینده نگر مبتنی بر پرسشنامه بر روی بیماران POTS (n = 65) و افراد سالم (n = 95) نشان داد که سرگیجه در چرخه قاعدگی نوسان دارد، با بیشترین سبکی سر در طول قاعدگی، کاهش در فاز فولیکولی، کمترین آن در اواسط دوره قاعدگی و افزایش در اواخر فاز لوتئال. مطالعات در بیماران POTS (n = 65 و n = 191) افزایش خونریزی رحمی ، آمنوره ثانویه، فیبروم رحم (۲۵٪ در مقابل ۱۰٪ از افراد سالم)، آندومتریوز، کیست تخمدان (۴۳٪ در مقابل ۱۳٪ از افراد سالم) و سندرم احتقان لگن در بیماران POTS را نشان داده اند. یک مطالعه نظرسنجی مقطعی روی ۳۶۵۲ بیمار POTS که حداقل یک بارداری را گزارش کرده بودند، نشان داد که ۸۱٪ علائم بدتر شدن علائم را در طول بارداری گزارش کردند، در حالی که زیرمجموعه بیماران در سایر مطالعات کوچک بهبود علائم را گزارش کردند. مشابه ME/CFS، ۹ درصد از بیماران POTS (1933=n) در یک مطالعه مبتنی بر نظرسنجی مقطعی گزارش دادند که حاملگی باعث تحریک POTS آنها شده است.
۳.۳. سندرم اهلرز-دانلوس (EDS)، اختلالات بافت همبند (CTDs) و سلامت باروری
تقریباً ۲۳٪ از بیماران LC ممکن است در یک فنوتیپ عضلانی-اسکلتی و سیستم عصبی قرار بگیرند که تا حدودی با شیوع بالاتر اختلالات بافت همبند (CTDs) مشخص می شود که این مساله با یک مطالعه EHR روی بیش از ۳۴۰۰۰ بیمار LC مشخص شده است. مرکز کنترل و پیشگیری از بیماری های ایالات متحده درگیری سیستمیک بافت همبند را به عنوان یک بیماری مرتبط با کووید-۱۹ شناسایی کرده است. در حالی که شیوع CTDs در LC هنوز مشخص نشده است، مطالعات موردی نشان میدهد که برخی از بیماران پس از COVID-19 دچار بیش حرکتی مفصل میشوند. CTD ها، از جمله EDS و بزرگترین زیرگروه EDS هایپرموبایل آن (hEDS)، در بیماران مبتلا به ME/CFS و POTS نسبتاً رایج هستند. علائم hEDS شامل سابلوکساسیون مفصل، کشیدگی پوست، درد و خستگی و همچنین تظاهرات قلبی عروقی، گوارشی، عصبی و اسکلتی عضلانی است. شیوع دقیق در مطالعات مختلف متفاوت است، اما برخی دریافتند که تا ۳۱٪ از بیماران POTS (n = 91) و ۲۰٪ از بیماران ME/CFS دارای hEDS (n = 229) هستند. مطرح کردن تشخیص میتواند سالها طول بکشد و hEDS معیارهای تشخیصی دقیقی دارد، بنابراین شیوع کلی CTDs در این بیماریها ممکن است بیشتر از آن چیزی باشد که آمار hEDS نشان میدهد. در حالی که مکانیسم های CTD ها، به ویژه در رابطه با بیماری مزمن مرتبط با عفونت، مورد تحقیق قرار نگرفته است، برخی از محققان گمان می کنند که فعال سازی ماست سل (MCA) ممکن است در برخی از CTD ها دخیل باشد، زیرا واسطه های ماست سل مانند تریپتاز و هیستامین می توانند به کلاژن آسیب برسانند. قابل ذکر است که علائم MCA در بیماران LC شایع است و میزان قابل توجهی از همراهی تشخیصی بین سندرم فعال سازی ماست سل (MCAS) و EDS، ME/CFS و POTS وجود دارد. علائم قاعدگی در بیماران EDS می تواند شدید باشد: ۵۰% -۷۶% (n = 26، n = 386، n = 1352) منوراژی (قاعدگی های سنگین) را گزارش می دهند. ۷۲٪ (n = 386) دیسمنوره (دردهای قاعدگی)، ۴۰٪ (n = 1352) دیسمنوره شدید را گزارش کردند، ۱۶% (۱۳۵۲=n) درد متوسط تا شدید را تجربه کردند و ۳۱% (۱۳۵۲=n) خونریزی بین قاعدگی دارند (مطالعات فاقد کنترل هستند). علاوه بر این، ۴۳٪ – ۶۴٪ (n = 386، و n = 1146) از بیماران EDS دیسپارونی (مقاربت دردناک) و ۵۰٪ (۱۱۴۶=n) ولوودینیا (درد در اطراف واژن) را گزارش کردند.
عوارض جدی بارداری در بیماران مبتلا به EDS و CTD شایع است، اما کمتر از نیمی از آنها در مورد این خطرات مطلع هستند. در یک مطالعه گذشته نگر ۱۶ ساله مبتنی بر جمعیت، بارداری در بیماران EDS با نرخ بالاتری از پیامدهای نامطلوب، از جمله زایمان زودرس، نارسایی دهانه رحم، خونریزی قبل از زایمان، جفت سرراهی، سزارین، بستری طولانیتر پس از زایمان ، IUGR و مرگ مادر بود. در یک مطالعه بر روی ۱۳۵۲ زن مبتلا به EDS بدون کنترل، ۴۳.۳ درصد ناباروری را تجربه کردند. ۵۴.۵ درصد از کسانی که باردار بوده اند حداقل یک بار سقط جنین را تجربه کرده اند و ۲۹.۶ درصد از کسانی که زایمان کرده بودند حداقل یک بار زایمان زودرس داشتند. مطالعات متعدد نشان داده است که در مقایسه با جمعیت عمومی، زنان مبتلا به سه نوع شایع EDS، میزان بیشتری از سقط جنین ، مردهزایی و پارگی زودرس پردهها (PPROM) دارند.
۳.۴. اندومتریوز
بر اساس یک مطالعه با استفاده از داده های پرونده الکترونیکی سلامت بیماران LC غیر بستری بیماران آندومتریوز ممکن است خطر ابتلا بیشتری به LC را داشته باشند. (aHR = 1.19، ۹۵% فاصله اطمینان (CI): 1.11-1.28) با این حال، تحقیقات بیشتری برای درک عوامل کمک کننده مورد نیاز است. اندومتریوز یک بیماری مزمن سیستمیک است که در آن بافتی شبیه به پوشش داخلی رحم در خارج از رحم رشد می کند. این بیماری ۱۰ درصد از دختران و زنان در سنین باروری و همچنین دختران قبل از یائسگی و زنان یائسه را تحت تاثیر قرار می دهد. آندومتریوز میتواند با طیفی از علائم شدید و ناتوانکننده، از جمله درد همراه با قاعدگی یا دخول، درد مزمن، ناباروری، خستگی، و با حوادثی مانند پره اکلامپسی و سایر پیامدهای نامطلوب بارداری همراه باشد. تشخیص تهاجمی جراحی و بافت شناسی، که به طور گسترده به عنوان استاندارد طلایی برای تشخیص استفاده میشود ، عدم آگاهی پزشک و نرمال سازی علایم توسط بیمار میتواند طور متوسط تشخیص را تا ۱۱ سال به تاخیر بیاندازد. که ممکن است درک شیوع آندومتریوز در LC را کاهش دهد. تقریباً ۳۶٪ از زنان مبتلا به ME/CFS (n = 36) و ۲۰٪ از زنان مبتلا به POTS (n = 65) اندومتریوز را گزارش می کنند. کاهش عملکرد سیتوتوکسیک سلول های کشنده طبیعی، تغییرات ماکروفاژها، کاهش کورتیزول، افزایش استرس اکسیداتیو و آلرژی ها در اندومتریوز و همچنین در ME/CFS نقش دارند که همپوشانی ها و نقش سیستم های ایمنی و غدد درون ریز ناکارآمد را در هر دو بیماری برجسته می کند. برخی از این مکانیسم ها ممکن است در LC نیز نقش داشته باشند. با وجود شیوع و ناتوانی ناشی از آندومتریوز، پاتوژنز آن ناشناخته باقی مانده است. یک فرضیه کمتر شناخته شده و کمتر بررسی شده پیشنهاد می کند که میکروب ها ممکن است از طریق یک پاسخ التهابی و فعال شدن TLR4 و TLR2 در اتیوپاتولوژی اندومتریوز (به عنوان مثال، “فرضیه آلودگی باکتریایی”) نقش داشته باشند. این تحقیق در زمینه مطالعات بر روی پاتوژن ها در بیماری های مزمن مرتبط با عفونت و اینکه چگونه آنها ممکن است در پاتولوژی های متعدد نقش داشته باشند قابل توجه است.
۴. بحث
تحقیقات در مورد RH در LC، علیرغم علائم گزارش شده توسط بیمار و اثرات مستند در LC و شرایط مرتبط، به مقادیر کافی وجود ندارد. مطالعات ذکر شده در این بررسی برای همه بیماریها عمدتاً مطالعات مقطعی، گزارشهای موردی، و فاقد گروههای کنترل سالم یا دیگر موارد مرتبط بودهاند .شرایطRH زنان به طور گسترده تر انجام شده است، اما RH و بیماری های مذکور در این مطالعه کمتر مورد تحقیق قرار گرفته است و بودجه تحقیقاتی بیشتری باید برای مطالعه RH در LC و بیماری های مرتبط با آن اختصاص داده شود. ما از محققان میخواهیم اولویتهای تحقیقاتی RH زیر را بررسی کنند و مطالعاتی را طراحی کنند که بیماریهای مرتبط با هم تداخل دارند (شکل ۲). از آنجا که عوامل خطر برای ایجاد LC ممکن است شامل جنسیت زن، محرومیت اجتماعی-اقتصادی، و هویت اقلیت نژادی/قومی باشد، این سوالات به طور ایدهآل از طریق مطالعات کوهورت طولی آیندهنگر کنترلشده و کارآزماییهای بالینی بررسی میشوند. ۷۰٪ تا ۸۰٪ از بیماران مبتلا به ME/CFS، POTS و EDS زن هستند. بنابراین، نقش جنسیت کروموزومی، هورمونی و آناتومیکی برای کشف درک چگونگی غالب شدن این بیماری ها در بیماران زن، بدتر شدن با چرخه قاعدگی و یائسگی حیاتی است. بررسی اینکه چگونه چرخه قاعدگی می تواند باعث تشدید علائم شود بسیار مهم است،
به ویژه:
(۱) مکانیسم های شعله ور شدن در زمان های مختلف چرخه قاعدگی (به عنوان مثال، اینکه آیا قاعدگی می تواند باعث ایجاد PEM شود یا خیر).
(2) چه قاعدگی و چه هورمون های جنسی زنانه (و احتمالاً داروهای ضد بارداری مصنوعی)، انعقاد بیش از حد را در LC و ME/CFS افزایش می دهند. میکروکلوت های فیبرینالوئید در ۱۰۰ درصد بیماران LC (70 نفر) و همچنین در بیماران ME/CFS (25 نفر) یافت شد. آنها مشکوک به دخالت این مساله در پاتوژنز، هیپوپرفیوژن و اختلال عملکرد عروقی هستند. جالب اینجاست که هورمونهای جنسی از جمله استروژن و پروژسترون دارای خاصیت انعقادی بیش از حد فیبرینوژن هستند. بنابراین، ما تحقیق در مورد اینکه آیا هورمون های جنسی بر انعقاد بیش از حد و میکرولخته شدن در LC و ME/CFS تأثیر می گذارند یا خیر را توصیه می کنیم.
(۳) ارتباط بین بیان ACE2، ماندگاری ویروسی و RH.
بیان ACE2 در دستگاه تناسلی در طول چرخه قاعدگی در نوسان است و ماندگاری ویروسی یکی از مکانیسم های فرضی است که به پاتوفیزیولوژی LC کمک می کند.
(۴) اینکه آیا نوسانات مربوط به چرخه قاعدگی در عدم استحکام بافت همبند در بیماران LC مبتلا به CTD تشدید می شود؟ زیرا استحکام مفاصل و بافت همبند زنانه ممکن است با هورمون ها در طول چرخه قاعدگی، به ویژه استرادیول، نوسان داشته باشد.
(۵) نوسانات MCA در طول چرخه قاعدگی و نقش MCA مزمن، به ویژه MCA مزمن ناشی از عفونت، در شرایط RH مهم است(به عنوان مثال، MCA ممکن است در پاتوفیزیولوژی و علائم آندومتریوز و همچنین در پره اکلامپسی دخیل باشد).
(۶) میکروبیوم های واژن و تغییرات ان در قاعدگی و LC و تأثیر آنها بر RH. دیس بیوز میکروبیوم یک عامل آسیب شناسی پیشنهادی LC است.
(۷) با توجه به شواهد مبنی بر یائسگی زودرس و تشدید علائم در زنان یائسه ،باید بررسی کرد که علائم یائسگی چه تاثیر بر تشدید بیماری دارد.
بارداری
با توجه به اینکه برخی از بیماران ME/CFS و POTS بهبود کامل یا بهبودی علائم را در طول و بعد از بارداری گزارش میکنند، در حالی که برخی دیگر بدتر شدن علائم یا شروع بیماری جدید با بارداری را گزارش میکنند باید اثر بارداری بر این مساله را بررسی کرد. علاوه بر این، با پیشرفت تحقیقات، پزشکانی که با بیماران مبتلا به LC که باردار هستند یا قصد بارداری دارند، کار می کنند باید از خطرات بالقوه مرتبط با بارداری، به ویژه برای بیماران مبتلا به CTD آگاه باشند و در مورد آنها صحبت کنند.
غربالگری بیماری های همراه و بیماری های مرتبط با کووید طولانی مدت
مراقبت های توانبخشی و تحقیقات بر روی بیماران LC باید شامل غربالگری علائم و شرایط RH (به عنوان مثال، اندومتریوز)، و همچنین بیماری های دارای همپوشانی مانند ME/CFS، POTS، CTDs و موارد دیگر باشد تا آنجا که ما می دانیم، هیچ مطالعه منتشر شده ای برای بررسی اختلال نارسایی پیش از قاعدگی (PMDD) و/یا اختلال عملکرد جنسی زنان به دنبال عفونت COVID-19 [در مقایسه با ۶۰ مطالعه در مورد اختلال نعوظ پس از عفونت COVID-1] وجود ندارد. همچنین بررسی اینکه آیا پاتولوژی های مرتبط با LC خطر سرطان در دستگاه تناسلی را از طریق مکانیسم هایی مانند دیس بیوز ناشی از عفونت، التهاب مزمن، و ارتقای مسیرهای انکوژنیک افزایش می دهد یا خیر، حیاتی خواهد بود.
بیماری مزمن مرتبط با عفونت فراتر از کووید طولانی.
فقدان بحث در مورد سایر بیماریهای مزمن مرتبط با عفونت و شروع بیماری ناشی از تزریق واکسن به دلیل عدم ارتباط آنها نیست، بلکه به دلیل عدم وجود تحقیقات در مورد تأثیرات RH آنها است. گنجاندن این جمعیت بیماران (به عنوان مثال، بیماری مزمن لایم) در تحقیقات آینده برای درک بیماری های مزمن مرتبط با عفونت در سراسر محرک های آنتی ژن مفید خواهد بود.
نابرابری های سلامت در تحقیقات.
مطالعات بررسی شده عمدتاً جمعیتهای سفیدپوست را در کشورهای با درآمد بالا مورد مطالعه قرار میدهد که ممکن است این بیماریها به طور سیستماتیک در میان افراد گروههای به حاشیه رانده شده کمتر تشخیص داده شود . تحقیقات بالینی از لحاظ تاریخی فاقد بازنمایی مناسب نژادی/قومی/جنسیتی به دلیل موانع مشارکت و نژادپرستی سیستمی و نهادی در مراقبت های بهداشتی بوده است. برای ارتقای برابری سلامت و مقابله با نژادپرستی و سوگیری در تحقیقات بهداشتی، مطالعات باید توجه به این مسایل را در اولویت قرار دهند. علاوه بر این، تمرکز مطالعات بر روی تجربیات RH در جمعیت LC که در کشورهای با درآمد کم و متوسط (LMIC) زندگی می کنند، مهم خواهد بود، زیرا فراوانی و تأثیر اختلالات قاعدگی در بین بزرگسالان و نوجوانان در این کشورها حتی قبل از COVID بالاتر بود. فقدان تحقیق و بودجه ناکافی تحقیقات برای شرایط RH و بیماریهای مزمن مرتبط با عفونت ، کاستیهای مراقبتهای بالینی را تشدید میکند و تفاوتهای جنسیتی و نژادی/قومی به این کاستیها می افزاید. بیماران مبتلا به LC اغلب احساس میکنند که توسط پزشکان نادیده گرفته شدهاند که با توجه به تاخیرهای تشخیصی گسترده و میزان بالایی از تشخیص اشتباه اولیه ا. با ادامه یافتن کووید-۱۹، تعداد بیماران مبتلا به LC همچنان در حال افزایش است، اما تحقیقات کمی در مورد پیامدهای RH زنانه LC وجود دارد. LC ممکن است با اختلال در چرخه قاعدگی، عملکرد غدد جنسی، نارسایی تخمدان، یائسگی زودرس و مشکلات باروری همراه باشد. شرایط RH مرتبط با بیماریهای مرتبط (مانند ME/CFS، POTS، EDS) شامل دیسمنوره، آمنوره، الیگومنوره، دیسپارونی، اندومتریوز، ناباروری، ولوودینیا، خونریزی بین قاعدگی، کیستهای تخمدان، خونریزی لگنی و فیبروم رحمی عوارضی مانند مرگ و میر مادر، پره اکلامپسی و زایمان زودرس میشود. شرایط RH بر کیفیت زندگی تأثیر منفی می گذارد و بسیاری از زنان و دختران را از مشارکت کامل در اقتصاد و جامعه باز می دارد. ما به محققان، بیماران و پزشکان توصیه می کنیم که آینده بهتری را برای تحقیقات در مورد اثرات RH، LC و بیماری های مرتبط با آن شکل دهند.